题目内容
【题目】下列实验操作或事故处理正确的是
A.金属Na着火,立即用水扑灭
B.实验结束后,用嘴吹灭酒精灯
C.皮肤上不慎沾上浓NaOH溶液,立即用盐酸冲洗
D.稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断搅拌
【答案】D
【解析】A.钠与水发生反应生成可燃性的氢气,因此金属钠着火,不能用水灭,应用沙子盖灭,故A错误;B.实验结束,若用嘴吹灭酒精灯,易引起酒精灯内酒精蒸气着火,故B错误;C.盐酸有腐蚀性,应用大量水冲洗,故C错误;D.稀释浓硫酸时,应将浓硫酸沿容器壁慢慢注入水中,不能将水注入浓硫酸中,故D正确。故选D。

练习册系列答案
相关题目
【题目】氯化铁是常见的水处理剂,工业上制备无水FeCl3的一种工艺如图: 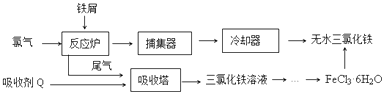
(1)由FeCl36H2O晶体制备无水FeCl3应采取的措施是: .
(2)六水合氯化铁在水中的溶解度如下:
温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
溶解度(g/100gH2O) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
从FeCl3溶液制得FeCl36H2O晶体的操作步骤是:加入少量盐酸、、、过滤、洗涤、干燥.
(3)常温下,若溶液的pH控制不当会使Fe3+沉淀,pH=4时,溶液中c(Fe3+)=molL﹣1 . (常温下Ksp[Fe(OH)3]=2.6×10﹣39)
(4)FeCl3的质量分数通常可用碘量法测定:称取2.300g无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入某一指示剂并用0.1000molL﹣1Na2S2O3溶液滴定用去12.50mL.
已知:I2+2S2O32﹣=2I﹣+S4O62﹣
①写出加入稍过量的KI溶液反应的离子方程式.
②求样品中氯化铁的质量分数(写出计算过程)