题目内容
某混合气体G可能含有CO、CO2、SO2、H2O等气体,用a.无水CuSO4,b.澄清石灰水,c.灼热CuO,d.碱石灰,e.酸性品红溶液,f.酸性高锰酸钾溶液等药品可将其一一检出,检出的正确顺序是( )。
| A.G→a→e→b→f→d→c |
| B.G→c→d→b→e→f→a |
| C.G→a→e→f→b→d→c |
| D.G→b→e→f→a→d→c |
C
首先用无水CuSO4检验水,然后用酸性品红溶液检验SO2,因为SO2和CO2均使澄清石灰水变浑浊,所以应用酸性KMnO4除去SO2后再用澄清石灰水检验CO2,最后用碱石灰干燥剩余气体后,再用灼热CuO检验CO的存在。

练习册系列答案
相关题目
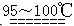 S2Cl2。
S2Cl2。