题目内容
将0.03 mol Cl2缓缓通入含有0.02 mol H2SO3和0.02 mol HBr的混合液中,则溶液中H+的浓度与通入氯气的物质的量的关系是下列图中的(纵坐标都表示氢离子的物质的量浓度) ( )。


B
H2SO3的还原性比HBr强,故向二者的混合液中通入氯气时,H2SO3先被氧化:H2SO3+Cl2+H2O=H2SO4+2HCl,c(H+)将增大,直至H2SO3被消耗完;继续通入氯气,氯气置换出溴:Cl2+2HBr=2HCl+Br2,此时溶液中H+的浓度基本不变。

练习册系列答案
相关题目
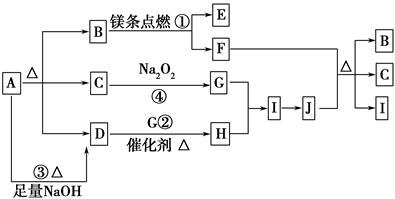
 2MgO+C,请填写以下空白:
2MgO+C,请填写以下空白: