题目内容
【化学--选修2化学与技术】(15分)
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
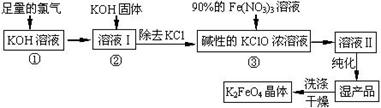
已知:2KOH + Cl2 ═ KCl + KClO + H2O(条件:温度较低)
6KOH + 3Cl2 ═ 5KCl + KClO3 + 3H2O(条件:温度较高)
回答下列问题:
(1)该生产工艺反应①应在 (填“温度较高”或“温度较低”)的情况下进行;
(2)写出工业上制取Cl2的化学方程式 ;
(3)K2FeO4具有强氧化性的原因 ;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体( 该溶液的密度为1.47 g/mL),它
的物质的量浓度为 ;
(5)在“溶液I”中加KOH固体的目的是 :
(6)从“反应液II”中分离出K2FeO4后,还会有副产品 (写化学式),它们都是重要的化工 产 品,具体说出其中一种物质的用途 (答1点即可); 则反应③中发生的离子反应方程式为 。
(7)如何判断K2FeO4晶体已经洗涤干净 。
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:

已知:2KOH + Cl2 ═ KCl + KClO + H2O(条件:温度较低)
6KOH + 3Cl2 ═ 5KCl + KClO3 + 3H2O(条件:温度较高)
回答下列问题:
(1)该生产工艺反应①应在 (填“温度较高”或“温度较低”)的情况下进行;
(2)写出工业上制取Cl2的化学方程式 ;
(3)K2FeO4具有强氧化性的原因 ;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体( 该溶液的密度为1.47 g/mL),它
的物质的量浓度为 ;
(5)在“溶液I”中加KOH固体的目的是 :
| A.与 “溶液I” 中过量的Cl2继续反应,生成更多的KClO |
| B.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
| C.为下一步反应提供反应物 |
| D.使副产物KClO3转化为 KClO |
(7)如何判断K2FeO4晶体已经洗涤干净 。
(15分)
(1)温度较低 (1分)
(2)2NaCl + 2H2O 2NaOH + H2↑ + Cl2↑(2分)
2NaOH + H2↑ + Cl2↑(2分)
(3)Fe元素的化合价显+6价,易得电子(1分)
(4)10 mol/L (2分)
(5)AC (2分)
(6)KNO3 KCl, (2分)
KNO3可用于化肥,炸药等 (答1点即得1分)
2Fe3+ + 3ClO- + 10 OH- = 2FeO42- + 3Cl-+ 5H2O (2分)
(7)取最后一次的洗涤液于试管中,先加稀硝酸、再加硝酸银溶液,无白色沉淀则已被洗净,反之则沉淀没有洗涤干净。(2分)
(1)温度较低 (1分)
(2)2NaCl + 2H2O
 2NaOH + H2↑ + Cl2↑(2分)
2NaOH + H2↑ + Cl2↑(2分)(3)Fe元素的化合价显+6价,易得电子(1分)
(4)10 mol/L (2分)
(5)AC (2分)
(6)KNO3 KCl, (2分)
KNO3可用于化肥,炸药等 (答1点即得1分)
2Fe3+ + 3ClO- + 10 OH- = 2FeO42- + 3Cl-+ 5H2O (2分)
(7)取最后一次的洗涤液于试管中,先加稀硝酸、再加硝酸银溶液,无白色沉淀则已被洗净,反之则沉淀没有洗涤干净。(2分)
试题分析:(1)该生产工艺反应①应在较低温度下进行,因为后面会用到KClO溶液;
(2)工业上制取Cl2,是通过电解饱和食盐水的方法,化学方程式为2NaCl + 2H2O
 2NaOH + H2↑ + Cl2↑;
2NaOH + H2↑ + Cl2↑;(3)K2FeO4具有强氧化性的原因是Fe元素的化合价显+6价,易得电子,具有强氧化性;
(4)溶液的质量是100+61.6=161.6g,则溶液的体积为161.6g/1.47g/mL=110mL=0.11L,溶质的物质的量是61.6g/56g/mol=1.1mol,所以溶液的物质的量浓度为1.1mol/0.11L=10mol/L;
(5)反应①中通入过量的氯气,所以氯气有剩余,加入氢氧化钾固体与过量的氯气反应,生成更多的KClO,为下一步反应提供反应物;所以答案选AC;
(6)反应③中硝酸铁与次氯酸钾发生氧化还原反应,铁离子被氧化为FeO42- ,次氯酸根离子被还原为氯离子,所以从“反应液II”中分离出K2FeO4后,还会有副产品KNO3、KCl,其中KNO3可用于化肥,炸药等;根据分析,反应③中发生的离子反应方程式为2Fe3+ + 3ClO- + 10 OH- = 2FeO42- + 3Cl-+ 5H2O;
(7)生成K2FeO4的同时还有氯化钾生成,所以判断K2FeO4晶体是否洗涤干净就是判断洗涤液中是否含有氯离子,判断方法是取最后一次的洗涤液于试管中,先加稀硝酸、再加硝酸银溶液,无白色沉淀则已被洗净,反之则沉淀没有洗涤干净。2FeO4晶体洗涤干净的方法

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 CO2(g)+H2(g)
CO2(g)+H2(g)