题目内容
14.某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,则下列四种说法正确的个数为( )①溶液甲中一定含Al(NO3)3和 Zn(NO3)2
②固体乙中一定含Ag,可能含有Cu和Zn
③若溶液甲呈蓝色,则溶液甲一定含Al(NO3)3、Zn(NO3)2、Cu(NO3)2和AgNO3
④若向固体乙上滴加盐酸无气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2.
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
分析 根据在金属活动性顺序中,排在前面的金属可以把位于它后面的金属从其盐溶液中置换出来,可简记为“前置后,盐可溶”.
解答 解:金属活动性Al>Zn>Cu>Ag,所以锌粉优先与AgNO3发生反应,铜粉后与AgNO3发生反应,但是铜粉和锌粉都不能和Al(NO3)3发生反应,Al(NO3)3一定在溶液中;
①锌粉优先与AgNO3发生反应生成硝酸锌和银,铜粉和锌粉都不能和Al(NO3)3发生反应,所以溶液中一定有Al(NO3)3和Zn(NO3)2,故说①法正确;
②锌粉优先与AgNO3发生反应生成硝酸锌和银,固体乙中一定含有Ag,可能有Cu和Zn,故②说法正确;
③若溶液甲是蓝色,说明铜已经与AgNO3发生反应,而锌已经全部反应,溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2,AgNO3的存在不能确定,故③说法不正确;
④向固体乙上滴加盐酸无气泡产生,说明固体中没有锌,锌可能过量\适量或不足,不能说明AgNO3和Cu(NO3)2的存在.故④说法不正确;
由上述分析可知,正确的是2个,
故选:B.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行,掌握基础是关键,题目较简单.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案
相关题目
4.从某海洋动物体中可以提取具有抗肿瘤的活性天然产物,实验小组按以下实验方案进行:
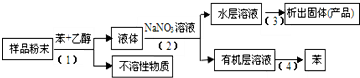
下列说法错误的是( )

下列说法错误的是( )
| A. | 步骤(3)需要用到坩埚 | B. | 步骤(2)需要用到分液漏斗 | ||
| C. | 步骤(1)需要过滤装置 | D. | 步骤(4)需要蒸馏装置 |
5.下列叙述正确的是( )
| A. | 1 mol H2O的质量为18 g/mol | |
| B. | CH4的摩尔质量为16 g | |
| C. | 3.01×1023个SO2分子的质量为32g | |
| D. | 标准状况下,1 mol任何物质体积均为22.4 L |
2.下列除去杂质的方法(括号里为少量杂质)中,所用试剂或操作不正确的是( )
| A. | NaHCO3溶液(Na2CO3):通入过量的CO2 | |
| B. | CO2(HCl):将气体通过盛有饱和Na2CO3溶液的洗气瓶 | |
| C. | SiO2(Al2O3):加入稀盐酸再过滤 | |
| D. | FeCl3溶液(FeCl2):通入足量的氯气 |
9.下列电子式书写不正确的是( )
| A. | HCl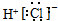 | B. | CaCl2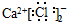 | C. | BaCl2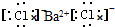 | D. | NaOH 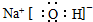 |
19.下列关于分子间作用力的说法,正确的是( )
| A. | 分子间作用力是一种比较弱的化学键 | |
| B. | 氯化钠晶体中不存在范德华力 | |
| C. | 锂、钠、钾、铷、铯的熔点越来越低是因为分子间作用力越来越弱 | |
| D. | 分子间作用力越大,分子的热稳定性就越大 |
6.下列说法正确的是( )
| A. | SO3溶解于水时能导电,所以SO3是电解质 | |
| B. | 离子化合物中不存在独立的分子 | |
| C. | 稀硝酸能导电,所以HNO3溶液属于电解质 | |
| D. | 熔融时能导电的物质一定是电解质 |
3.如图所示为4种氨基酸的结构式,则夏利叙述正确的是( )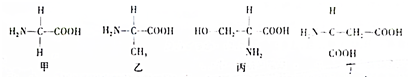
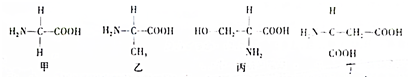
| A. | 构成氨基酸的元素只有C、H、O、N4种 | |
| B. | 氨基酸丙和丁的R基分别是-NH3和-CH2-COOH | |
| C. | R基中可以有氨基或羧基 | |
| D. | 组成水稻的氨基酸包括必需氨基酸和非必需氨基酸 |