题目内容
19.下列关于物质性质的说法不合理的是( )| A. | SO2气体通入紫色石蕊试液中,溶液先变红后褪色 | |
| B. | FeCl3、Na2O2、Cu2S均可由相应单质直接化合生成 | |
| C. | 金属Mg与稀硫酸和CO2均能反应,其反应类型相同 | |
| D. | 氢氧化铝、碳酸铵、碳酸氢钠都既能与盐酸反应,又能与氢氧化钠溶液反应 |
分析 A.二氧化硫不能够漂白石蕊溶液;
B.铁与氯气反应生成氯化铁,钠与氧气在加热条件下生成过氧化钠,铜与硫反应生成硫化亚铜;
C.镁与硫酸反应生成硫酸镁和氢气,镁与二氧化碳反应生成碳和氧化镁;
D.两性物质、弱酸的酸式盐、弱酸的铵盐既能够与盐酸又能与氢氧化钠反应.
解答 解:A.SO2是酸性氧化物,也具有漂白性,但不能漂白指示剂,所以溶液只变红不褪色,故A错误;
B.铁与氯气反应生成氯化铁,钠与氧气在加热条件下生成过氧化钠,铜与硫反应生成硫化亚铜,故B正确;
C.镁与硫酸反应生成硫酸镁和氢气,镁与二氧化碳反应生成碳和氧化镁,二者都是置换反应,故C正确;
D.氢氧化铝、碳酸铵、碳酸氢钠分别是两性物质、弱酸的铵盐、弱酸的酸式盐,都能够与盐酸和氢氧化钠反应,故D正确;
故选:A.
点评 本题考查了元素化合物知识,熟悉物质的化学性质是解题关键,注意对既能够与盐酸又能与氢氧化钠反应物质的积累,题目难度不大.

练习册系列答案
相关题目
10.下列有关元素的性质或递变规律正确的是( )
| A. | ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 | |
| B. | 第三周期主族元素从左到右,氧化物对应的水化物酸性依次增强 | |
| C. | 同主族元素的简单阴离子还原性越强,对应的简单氢化物沸点越高 | |
| D. | 同周期金属元素的主族序数越大,其原子失电子能力越强 |
7.将2.3g钠放入97.7g水中,下列说法正确的是( )
| A. | 产生的气体含有0.1mol的电子 | B. | 电子转移的数目为2NA | ||
| C. | 所得溶液的质量分数是等于4% | D. | 产生气体的体积为1.12L |
14.下列说法正确的是( )
| A. | 向饱和食盐水中加入少量的浓盐酸,看不到明显的现象 | |
| B. | 将硫酸铜溶液与碳酸钠溶液混合,得到的沉淀是以Cu(OH)2为主,说明了在相同条件下Cu(OH)2的溶解度比CuCO3的更小 | |
| C. | 在0.01mol/L NaCl溶液中加入少量的AgNO3溶液,有白色沉淀生成,接着向上述溶液中加入足量的浓氨水,白色沉淀不会溶解 | |
| D. | CaCO3溶液的导电能力很弱,是因为CaCO3是弱电解质,存在如下电离平衡:CaCO3?Ca2++CO${\;}_{3}^{2-}$ |
11.常温下,下列各组离子或分子在指定溶液中能大量共存的是( )
| A. | pH=l的溶液中:Fe2+、Na+、S042-、N03- | |
| B. | 水电离的c(H+)=l×l0-13mol/L的溶液中:NH4+、K+、Cl-、HC03- | |
| C. | KMn04溶液中:H+、Na+、S042-、C2H50H | |
| D. | 使甲基橙变红色的溶液中:NH4+、Al3+、N03-、Cl- |
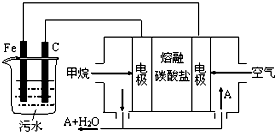 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,除去浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,除去浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.