题目内容
9.C、N、S都是重要的非金属元素.下列说法正确的是( )| A. | 三者对应的氧化物均为酸性氧化物 | |
| B. | 同浓度的Na2CO3、NaNO3、Na2SO3溶液的pH:NaNO3<Na2SO3<Na2CO3 | |
| C. | 三者的单质直接与氧气反应都能生成两种以上氧化物 | |
| D. | CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
分析 A.CO、NO是非成盐氧化物;
B.酸的酸性越强,其形成的钠盐碱性越弱;
C.氮气和氧气反应只能生成NO、S和氧气反应只能生成二氧化硫;
D.二氧化氮和水反应生成硝酸和NO,属于氧化还原反应.
解答 解:A.CO、NO是非成盐氧化物,但二氧化碳、五氧化二氮、二氧化硫等都是酸性氧化物,故A错误;
B.酸性HNO3>H2SO3>H2CO3,碳酸根离子水解程度大于亚硫酸根离子,硝酸根离子是强酸根离子,不水解,所以相同浓度的钠盐溶液pH:NaNO3<Na2SO3<Na2CO3,故B正确;
C.氮气和氧气反应只能生成NO、S和氧气反应只能生成二氧化硫,所以氮气、S和氧气反应只生成一种氧化物,故C错误;
D.二氧化氮和水反应生成硝酸和NO,属于氧化还原反应,二氧化碳、二氧化硫和水反应都生成一种化合物,且没有电子转移,故D错误;
故选B.
点评 本题考查非金属元素及其化合物,侧重考查元素化合物性质及基本概念、盐类水解等,注意二氧化氮和水反应属于氧化还原反应,注意A中某些氧化物是不成盐氧化物,为易错点.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
19.下列实验装置或操作不符合实验要求的是( )
| A. | 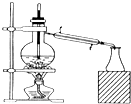 石油分馏 | B. | 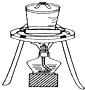 灼烧干海带 | ||
| C. | 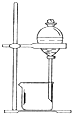 用CCl4提取碘水中的碘 | D. |  冶炼金属铁 |
20.下列有关实验原理、方法和结论都正确的是( )
| A. | 向某溶液中加入盐酸酸化的氯化钡溶液有白色沉淀生成,该溶液中一定含SO42- | |
| B. | 向蛋白质溶液中加入硫酸铜溶液,将得到的沉淀分离出来,再加水可重新溶解 | |
| C. | 除去苯中含有的苯酚,可先加NaOH溶液,充分反应后静置分液 | |
| D. | 淀粉和稀硫酸混合加热一段时间后,加入氢氧化钠使溶液呈碱性,再加入新制Cu(OH)2后加热,若有砖红色沉淀生成,则淀粉已经完全水解 |
18.X、Y、Z、W为四种短周期元素,已知X、Z同主族,Y、Z、W同周期;X的气态氢化物比Z的稳定;Y的阳离子比W的阳离子氧化性强;Y的阳离子比Z的阴离子少一个电子层.下列表示中,正确的是( )
| A. | 原子序数:X>Y>Z>W | B. | 简单离子半径:W>Y>Z>X | ||
| C. | 原子半径:W>Y>Z>X | D. | 原子的得电子能力:X<Z |
19.设NA为阿伏加德罗常数,下列叙述中不正确的是( )
| A. | 在28g聚乙烯中,含有的碳原子个数为2NA | |
| B. | 在合成28g聚乙烯的单体中,含有NA个碳碳双键 | |
| C. | 在28g聚乙烯中,含有C-H的数目为4NA | |
| D. | 28g聚乙烯完全燃烧时,转移电子数为3NA |


 ;
; 结构(含E)的有13种;E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为
结构(含E)的有13种;E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为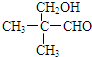 .
.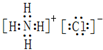 、用电子式表示⑥号物质的形成过程:
、用电子式表示⑥号物质的形成过程: .
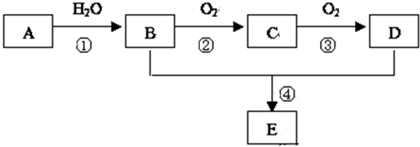
.
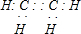 .
.