题目内容
【题目】NA是阿伏加德罗常数的值,下列说法正确的是
A. 36g由35Cl 和37C1组成的氯气中所含质子数一定为17NA
B. 7.8 g Na2O2与足量酸性KMnO4溶液反应,转移的电子数为0.2NA
C. 密闭容器中1mol PCl3与1 mol Cl2反应制备PCl5(g),增加了2NA个P-Cl键
D. 5.6g铁片投入足量浓硝酸中,转移的电子数为0.3 NA
【答案】B
【解析】
假设全是35Cl,则质子数是![]() ,假设全是37Cl,则质子数是
,假设全是37Cl,则质子数是![]() ;Na2O2与足量酸性KMnO4溶液反应,Na2O2只作还原剂,过氧化钠中氧元素化合价由-1升高为0,1mol过氧化钠转移2mol电子;PCl3与Cl2反应制备PCl5的反应可逆;常温下,铁在浓硝酸中钝化。
;Na2O2与足量酸性KMnO4溶液反应,Na2O2只作还原剂,过氧化钠中氧元素化合价由-1升高为0,1mol过氧化钠转移2mol电子;PCl3与Cl2反应制备PCl5的反应可逆;常温下,铁在浓硝酸中钝化。
假设全是35Cl,则质子数是![]() ,假设全是37Cl,则质子数是
,假设全是37Cl,则质子数是![]() ,根据极值法,36g由35Cl 和37C1组成的氯气中所含质子数不一定为17NA,故A错误;Na2O2与足量酸性KMnO4溶液反应,Na2O2只作还原剂,过氧化钠中氧元素化合价由-1升高为0,1mol过氧化钠转移2mol电子 ,所以7.8 g Na2O2与足量酸性KMnO4溶液反应,转移的电子数为0.2NA,故B正确;PCl3与Cl2反应制备PCl5的反应可逆,密闭容器中1mol PCl3与1 mol Cl2反应制备PCl5(g),生成PCl5(g)小于1mol, P-Cl键增加小于2NA个,故C错误;常温下,铁在浓硝酸中钝化,故D错误,选B。
,根据极值法,36g由35Cl 和37C1组成的氯气中所含质子数不一定为17NA,故A错误;Na2O2与足量酸性KMnO4溶液反应,Na2O2只作还原剂,过氧化钠中氧元素化合价由-1升高为0,1mol过氧化钠转移2mol电子 ,所以7.8 g Na2O2与足量酸性KMnO4溶液反应,转移的电子数为0.2NA,故B正确;PCl3与Cl2反应制备PCl5的反应可逆,密闭容器中1mol PCl3与1 mol Cl2反应制备PCl5(g),生成PCl5(g)小于1mol, P-Cl键增加小于2NA个,故C错误;常温下,铁在浓硝酸中钝化,故D错误,选B。

【题目】研究硫元素及其化合物的性质具有重要意义。
(1)25 ℃,在0.10 mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与[S2-]关系如下图(忽略溶液体积的变化、H2S的挥发)。
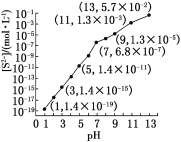
①pH=13时,溶液中的[H2S]+[HS-]=__________mol·L-1。
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH=____________时,Mn2+开始沉淀[已知:Ksp(MnS)=2.8×10-13]。
(2)25 ℃,两种酸的电离平衡常数如下表。
物质 | Ka1 | Ka2 |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO的电离平衡常数表达式K=________。
②0.10 mol·L-1Na2SO3溶液中离子浓度由大到小的顺序为____________________。
③H2SO3溶液和NaHCO3溶液反应的主要离子方程式为_________________________。