题目内容
【题目】X、Y、Z、W、R是周期表前四周期的五种元素,原子序数依次增大。X原子p轨道上有两个未成对电子;Y的气态氢化物能使石蕊试液变蓝色;Z的最外层电子数为其内层电子数的3倍;W的价电子排布式为ns(n-1)np2(n-1);R的最外层只有1个电子,次外层有18个电子。
(1)X、Y、Z、W四种元素中电负性最大的是__________(填元素符号),基态R原子的核外电子排布式为______________。
(2)X、Y、Z的最简单氢化物中,键角由大到小的顺序为_______________(用氢化物的化学式表示)。
(3)Z、W元素构成的微粒WZ42-的立体构型是________,与WZ42-互为等电子体的一种分子为____(填化学式,任写一种)。
(4)每个XY-离子中含有________个π键。
(5)已知Z、R能形成一种化合物R2Z,其晶胞结构如图所示。
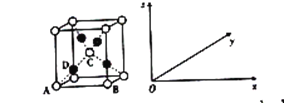
①该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为(![]() ,
, ![]() ,
, ![]() )。则D原子的坐标参数为________,它代表_______(填元素符号)原子。
)。则D原子的坐标参数为________,它代表_______(填元素符号)原子。
②若R2Z晶体密度dg·cm-3,晶胞参数为apm,则阿伏伽德罗常数值NA=______。
【答案】 O ls22s22p63s23p63d104s1(或[Ar] 3d104s1) CH4>NH3>H2O 正四面体 CCl4(或CF4、SiCl4、SiF4等) 2 (![]() ,
, ![]() ,
, ![]() ) Cu 288/(da3×10-30)
) Cu 288/(da3×10-30)
【解析】X的p轨道上有两个未成对电子,即属于IVA或VIA族元素,Y的气态氢化物能使石蕊试液变蓝,说明此氢化物是NH3,即Y为N,五种元素原子序数依次增大,即X为C,Z的最外层电子数为内层电子数的3倍,则Z为O,W的价电子排布式n-1应等于2,即n为3,则W为S,R的最外层只有1个电子,次外层有18个电子,即R为Cu,(1)本题考查电负性的规律和核外电子排布式,非金属性越强其电负性越大,同周期从左向右电负性增强,即电负性最强的是O,R位于第四周期IB族元素,其核外电子排布式为:ls22s22p63s23p63d104s1(或[Ar] 3d104s1);(2)本题考查影响键角的因素,氢化物分别是CH4、NH3、H2O,含有孤电子对数分别是0、1、2,孤电子对之间的斥力大于孤电子对-成键电子之间的斥力大于成键电子对之间的斥力,因此键角的大小是CH4>NH3>H2O;(3)本题考查空间构型和等电子体,组成的微粒是SO42-,中心原子S含有4个σ键,孤电子对数为(6+2-2×4)/2=0,空间构型为正四面体,等电子体是原子总数相等,价电子总数相等的微粒互为,与SO42-互为等电子体的是CCl4(或CF4、SiCl4、SiF4等);(4)考查化学键的类型和组成,构成的离子是CN-,C和N之间共用叁键,因此1个CN-中含有2个π键;(5)本题考查晶胞的坐标和晶胞的计算,①D的距离是A和C距离的一半,因此D原子的坐标为(![]() ,
, ![]() ,
, ![]() );A位于晶胞的顶点和体心,个数为8×1/8+1=2,D位于晶胞内部,有4个,因此化学式为Cu2O,即D为Cu;②晶胞的质量为2×144/NAg,体积为(a×10-10)3cm3,根据密度的定义,密度为d=2×144/(NA×a3×10-30)g/cm3,因此推出阿伏加德罗常数为288/(da3×10-30)。
);A位于晶胞的顶点和体心,个数为8×1/8+1=2,D位于晶胞内部,有4个,因此化学式为Cu2O,即D为Cu;②晶胞的质量为2×144/NAg,体积为(a×10-10)3cm3,根据密度的定义,密度为d=2×144/(NA×a3×10-30)g/cm3,因此推出阿伏加德罗常数为288/(da3×10-30)。

 阅读快车系列答案
阅读快车系列答案