��Ŀ����
19��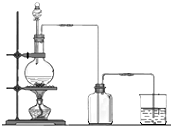 ʵ������MnO2��Ũ���ᷴӦ��ȡCl2�����巢�����ռ�װ����ͼ����ش�
ʵ������MnO2��Ũ���ᷴӦ��ȡCl2�����巢�����ռ�װ����ͼ����ش���1��ʵ��װ��������ɺ�����Ӧ���еIJ����Ǽ��װ�õ������ԣ�
��2��MnO2��Ũ���ᷴӦ��ȡCl2�Ļ�ѧ����ʽΪMnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��3��Ϊ�õ����������Cl2�����ռ�Cl2֮ǰӦ����ͨ��װ�б���ʳ��ˮ��Ũ���ᣨ���Լ����ƣ���ϴ��ƿ��
���� ��1����װ�����������������Բ���װҩƷ����ʵ�飻
��2������������Ũ�����ڼ��������·�Ӧ�����������Ȼ��̺�ˮ��
��3��Ũ�����ӷ��������Ʊ��������к����Ȼ��⡢ˮ��������������ڱ���ʳ��ˮ���ܽ�Ȳ����Ȼ���������ˮ��Ũ���������ˮ�Խ��
��� �⣺��1��ʵ��װ��������ɺ�����Ӧ���еIJ����ǣ����װ�õ������ԣ�
�ʴ�Ϊ�����װ�õ������ԣ�
��2������������Ũ�����ڼ��������·�Ӧ�����������Ȼ��̺�ˮ����ѧ����ʽ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��3��Ũ�����ӷ��������Ʊ��������к����Ȼ��⡢ˮ�����������ڱ���ʳ��ˮ���ܽ�Ȳ����Ȼ���������ˮ��ѡ��ʳ��ˮ��ȥ�Ȼ��⣬Ũ���������ˮ�ԣ����Ը���������
�ʴ�Ϊ������ʳ��ˮ��Ũ���ᣮ
���� ���⿼�����������Ʊ��;�������Ϥ�Ʊ�ԭ�������ʵ������ǽ���ؼ�����Ŀ�ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
9��X��Y��Z��W��������Ԫ�أ���X����������Y�������Ӿ�����ͬ�ĵ��Ӳ�ṹ��W�������ӵ������������ڵȵ������X�����ӵ�����������Z��Y��Ԫ�ص�����������Ӧ��ˮ����ķ���ʽ���ƣ������ߵ����Խ�ǰ��ǿ����������Ԫ�ص�ԭ�������ɴ�С������˳���ǣ�������
| A�� | X��W��Z��Y | B�� | W��X��Y��Z | C�� | Z��X��Y��W | D�� | X��Z��Y��W |
10���������ӷ���ʽ��ȷ���ǣ�������
| A�� | ��KAl��SO4��2��Һ�еμ�Ba��OH��2��Һ��Al3+ǡ�ó�����ȫ��2Al3++3SO42-+3Ba2++6OH-�T2Al��OH��3��+3BaSO4�� | |
| B�� | ��NH4HSO4��Һ�еμӹ���NaOH��Һ�����ȣ�NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$H2O+NH3�� | |
| C�� | ��AlCl3��Һ�еμӹ�����ˮ��Al3++4NH3?H2O�T[Al��OH��4]-+4NH4+ | |
| D�� | FeO����ϡ�����У�FeO+2H+�TFe2++H2O |
7��������Ԫ��M��N������M2+��N2-������ͬ���Ӳ�ṹ��������˵����ȷ���ǣ�������
| A�� | ������������M��N | B�� | ԭ��������M��N | ||
| C�� | ���Ӳ�����M=N | D�� | �뾶��M��N��M2+��N2- |
14�������й��Ҵ���˵���У�����ȷ���ǣ�������
| A�� | ������������ | B�� | ��Է�������Ϊ46 | ||
| C�� | �����к��еĹ��������ǻ� | D�� | �ڿ�������ȫȼ������CO2��H2O |
8�������й����ʵķ����У�����Ϊ�������ǣ�������
| A�� | Al��OH��3����������� | B�� | NH3•H2O����� | ||
| C�� | HClO ��ǿ�ᣩ | D�� | CuSO4•5H2O������ |
9�����ֶ�����Ԫ��A��B��C��D��E��Ԫ�����ڱ������λ����ͼ��ʾ������E�γɵ����������ﶼ�Ǵ�����Ⱦ����E�ĵ�����һ�ֻ�ɫ���壮
��1���û�ѧʽ��գ��Ƚ�A��D������������ȶ��ԣ�CH4��SiH4���Ƚ�D��E����������Ӧˮ��������ԣ�H2SO4��H2SiO3��
��2��B����̬�⻯����������������Ӧˮ������γ��Σ�������Һ�����ԣ�����ԡ��������ԡ����ԡ��������ӷ���ʽ��ʾ��ԭ��NH4++H2O?NH3��H2O+H+��
��3��д��CԪ��ԭ�ӵļ۵����Ų�ʽ��3s23p1�Ƚ�B��EԪ�ػ�̬ԭ�ӵĵ�һ�����ܴ�СN��S����Ԫ�ط�����գ���
��4��A����Ԫ���γ��������H����Ϊȼ�ϵ�ص�ԭ�ϣ�д����ȼ�ϵ�أ�������NaOH��Һ��Ϊ�������Һ�������缫��ӦCH4+10 OH--8e-=CO32-+7H2O��֪25��/101kPa�£�H��ȼ����Ϊ890kJ•mol-1��д��Hȼ���ȵĻ�ѧ����ʽ��CH4��g��+2O2��g��=CO2��g��+2H2O��l����H=-890kJ•mol-1��
��5����150ml��0.10•L-1���Ȼ�����Һ�м���40mLNaOH��Ҵ����ַ�Ӧ��õ�0.78g��������ԭNaOH��Һ�����ʵ���Ũ�ȿ�����0.75��1.5mol•L-1��
| A | B | ||
| C | D | E |
��2��B����̬�⻯����������������Ӧˮ������γ��Σ�������Һ�����ԣ�����ԡ��������ԡ����ԡ��������ӷ���ʽ��ʾ��ԭ��NH4++H2O?NH3��H2O+H+��
��3��д��CԪ��ԭ�ӵļ۵����Ų�ʽ��3s23p1�Ƚ�B��EԪ�ػ�̬ԭ�ӵĵ�һ�����ܴ�СN��S����Ԫ�ط�����գ���
��4��A����Ԫ���γ��������H����Ϊȼ�ϵ�ص�ԭ�ϣ�д����ȼ�ϵ�أ�������NaOH��Һ��Ϊ�������Һ�������缫��ӦCH4+10 OH--8e-=CO32-+7H2O��֪25��/101kPa�£�H��ȼ����Ϊ890kJ•mol-1��д��Hȼ���ȵĻ�ѧ����ʽ��CH4��g��+2O2��g��=CO2��g��+2H2O��l����H=-890kJ•mol-1��
��5����150ml��0.10•L-1���Ȼ�����Һ�м���40mLNaOH��Ҵ����ַ�Ӧ��õ�0.78g��������ԭNaOH��Һ�����ʵ���Ũ�ȿ�����0.75��1.5mol•L-1��
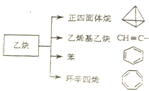 ��Ȳ��һ����Ҫ���л�����ԭ�ϣ�����ȲΪԭ���ڲ�ͬ�ķ�Ӧ�����¿���ת��������ʾ�ĸ��ֻ������ش�
��Ȳ��һ����Ҫ���л�����ԭ�ϣ�����ȲΪԭ���ڲ�ͬ�ķ�Ӧ�����¿���ת��������ʾ�ĸ��ֻ������ش�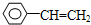 ��
��