题目内容
4. 已知Al2H6燃烧热极高,是一种很好的生氢剂,它跟水反应生成H2,球棍模型如图(白球为Al,黑球为H).下列推测肯定不正确的是( )
已知Al2H6燃烧热极高,是一种很好的生氢剂,它跟水反应生成H2,球棍模型如图(白球为Al,黑球为H).下列推测肯定不正确的是( )| A. | 该物质与水反应,属于氧化还原反应 | |
| B. | Al2H6在空气中完全燃烧,产物为氧化铝和水 | |
| C. | Al2H6分子中 氢为+1价,铝为-3价 | |
| D. | 氢铝化合物可能成为未来的储氢材料和火箭燃料 |
分析 A.Al2H6与水反应生成氢氧化铝和氢气,该反应中H元素化合价由-1价、+1价变为0价;
B.根据元素守恒分析;
C.根据元素的电负性和铝的化合价判断;
D.根据氢铝化合物的性质分析.
解答 解:A.Al2H6与水反应生成氢氧化铝和氢气,该反应中H元素化合价由-1价、+1价变为0价,所以属于氧化还原反应,故A正确;
B.根据题中信息Al2H6的燃烧热极高,判断Al2H6能燃烧,根据原子守恒,Al2H6的组成元素只有Al、H两种元素,又由于是在氧气中燃烧,推出燃烧产物为氧化铝和水,故B正确;
C.在化合物中电负性大的显负价,电负性小的元素显正价,氢元素的电负性大于铝元素,氢铝化合物中铝元素显+3价,氢元素显-1价,故C错误;
D.氢铝化合物能和水反应生成氢氧化铝和氢气,可以作储氢材料,燃烧热极高可以作火箭燃料,故D正确.
故选C.
点评 本题以铝的化合物为载体考查铝的化合物的性质,根据元素电负性、元素化合价和性质的关系来分析解答即可,侧重于考查学生对题目信息的提取和应用能力,题目难度中等.

练习册系列答案
相关题目
14.实验室模拟回收某废旧含镍催化剂(主要成份为NiO,另含Fe2O3、CaO、CuO、BaO等)生产Ni2O3.其工艺流程为如图1:
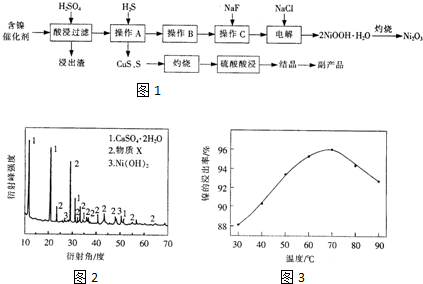
(1)根据图2所示的X射线衍射图谱,可知浸出渣含有三种主要成分,其中“物质X”为BaSO4.图3表示镍的浸出率与温度的关系,当浸出温度高于70℃时,镍的浸出率降低,浸出渣中Ni(OH)2含量增大,其原因是温度升高,Ni2+的水解程度增大.
(2)工艺流程中副产品的化学式为CuSO4•5H2O.
(3)已知有关氢氧化物开始沉淀和沉淀完全的pH如下表:
操作B是为了除去滤液中的铁元素,某同学设计了如下实验方案:向操作A所得的滤液中加入NaOH溶液,调节溶液pH为3.7~7.7,静置,过滤.请对该实验方案进行评价:方案错误,在调节pH前,应先在滤液中加入H2O2,使溶液中的Fe2+氧化为Fe3+(若原方案正确,请说明理由;若原方案错误,请加以改正).
(4)操作C是为了除去溶液中的Ca2+,若控制溶液中F浓度为3×10-3mol•L-1,则Ca2+的浓度为3×10-6mol•L-1.(常温时CaF2的溶度积常数为2.7×10-11)
(5)电解产生2NiOOH•H2O的原理分两步:①碱性条件下Cl-在阳极被氧化为ClO-;②Ni2+被ClO-氧化产生2NiOOH•H2O沉淀.第②步反应的离子方程式为ClO-+2Ni2++4OH-=2NiOOH•H2O↓+Cl-.

(1)根据图2所示的X射线衍射图谱,可知浸出渣含有三种主要成分,其中“物质X”为BaSO4.图3表示镍的浸出率与温度的关系,当浸出温度高于70℃时,镍的浸出率降低,浸出渣中Ni(OH)2含量增大,其原因是温度升高,Ni2+的水解程度增大.
(2)工艺流程中副产品的化学式为CuSO4•5H2O.
(3)已知有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
(4)操作C是为了除去溶液中的Ca2+,若控制溶液中F浓度为3×10-3mol•L-1,则Ca2+的浓度为3×10-6mol•L-1.(常温时CaF2的溶度积常数为2.7×10-11)
(5)电解产生2NiOOH•H2O的原理分两步:①碱性条件下Cl-在阳极被氧化为ClO-;②Ni2+被ClO-氧化产生2NiOOH•H2O沉淀.第②步反应的离子方程式为ClO-+2Ni2++4OH-=2NiOOH•H2O↓+Cl-.
15.下列表示或说法正确的是( )
| A. | 质子数为17、中子数为20的氯原子:${\;}_{17}^{20}$Cl | |
| B. | 等物质的量的水与重水含有相同数目的中子数 | |
| C. | 氯分子的电子式: | |
| D. | 恒温恒容条件下HI分解成气态I2的反应,体系的总压强保持不变时,说明反应处于平衡态 |
12.下列物质中属于油脂的是( )
| A. | 柴油 | B. | 羊油 | C. | 甘油 | D. | 汽油 |
19.把铁与铜的混合物放入稀HNO3中,反应后过滤,滤出的固体物质投入盐酸中无气体放出,则滤液里一定含有的金属盐是( )
| A. | Cu(NO3)2 | B. | Fe(NO3)3 | C. | Fe(NO3)2 | D. | Fe(NO3)2和Cu(NO3)2 |
13.下列叙述中正确的是( )
| A. | NH3、CO、CO2都是极性分子 | |
| B. | CH4、CCl4都是含有极性键的非极性分子 | |
| C. | HF、HCl、HBr、HI的稳定性依次增强 | |
| D. | 由于氢键的影响,H2O比H2S的稳定性更好 |

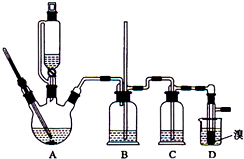 实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中发生如下反应:
实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中发生如下反应: