题目内容
18.关于阿伏加德罗常数的说法中错误的是( )| A. | 我们把0.012kg12C中所含的碳原子个数叫做阿伏加德罗常数 | |
| B. | 含的原子总数为6.02×1023个的CO,其物质的量为1mol | |
| C. | 凡是含有阿伏加德罗常数个微粒的集体,其物质的量就为1mol | |
| D. | 阿伏加德罗常数通常取6.02×1023mol-,常用NA表示 |
分析 A、0.012kg12C中所含的碳原子个数即为阿伏伽德罗常数;
B、CO为双原子分子;
C、将阿伏伽德罗常数个微粒看做一个整体即为1mol;
D、阿伏伽德罗常数的数值为6.02×1023,单位为mol-1.
解答 解:A、0.012kg12C中所含的碳原子个数即为阿伏伽德罗常数,将阿伏伽德罗常数个微粒看做一个整体即为1mol,故A正确;
B、CO为双原子分子,故当含6.02×1023个原子时,CO的物质的量为0.5mol,故B错误;
C、将阿伏伽德罗常数个微粒看做一个整体即为1mol,故凡是含有阿伏加德罗常数个微粒的集体,其物质的量就为1mol,故C正确;
D、阿伏伽德罗常数的数值为6.02×1023,单位为mol-1,即阿伏伽德罗常数为6.02×1023mol-1,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的定义和有关计算,掌握基础是关键,难度不大.

练习册系列答案
相关题目
8.分类是科学研究的重要方法,下列物质分类不正确的是( )
| A. | 化合物:干冰,冰水混合物,烧碱,小苏打 | |
| B. | 同素异形体:活性炭,C60,C80,金刚石 | |
| C. | 非电解质:乙醇,四氯化碳,氯气,葡萄糖 | |
| D. | 混合物:漂白粉,纯净矿泉水,盐酸,石灰石 |
9.下列有关胶体和溶液的比较中,正确的是( )
| A. | 溶液中溶质粒子不带电,胶体分散质粒子带电 | |
| B. | 溶液中溶质的粒子运动有规律,胶体粒子运动无规律 | |
| C. | 通直流电后,溶液中溶质的粒子分别向两极运动,而胶体中分散质的粒子向某一极运动 | |
| D. | 溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现光亮的“通路” |
6.根据下列反应判断有关物质还原性由强到弱的顺序是( )
H2SO3+I2+H2O═2HI+H2SO4 2FeCl3+2HI═2FeCl2+2HCl+I2
3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
H2SO3+I2+H2O═2HI+H2SO4 2FeCl3+2HI═2FeCl2+2HCl+I2
3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
| A. | NO>FeCl2>H2SO3>HI | B. | HI>FeCl2>H2SO3>NO | ||
| C. | FeCl2>HI>H2SO3>NO | D. | H2SO3>HI>FeCl2>NO |
13.下列操作不正确的是( )
| A. | 配制物质的量浓度的溶液,在定容时滴加蒸馏水超过刻度线,可用滴管吸出一部分使其溶液的凹液面与刻度线相切 | |
| B. | 过滤的时候,用玻璃棒引流,并将玻璃棒与三层滤纸的边缘接触 | |
| C. | 试管中滴加溶液时,不能将滴管伸入试管口内,应悬空滴入 | |
| D. | 蒸发氯化钠溶液,待蒸发皿中有大量固体出现时,停止加热,用余热蒸干 |
3.下列溶液中与50mL 1mol•L-1的AlCl3溶液中氯离子浓度相等的是( )
| A. | 150mL1mol•L-1 的NaCl | B. | 75mL2 mol•L-1 的NH4Cl | ||
| C. | 150mL3mol•L-1的KCl | D. | 75mL2mol•L-1的CaCl2 |
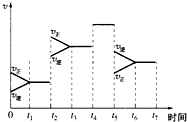 有A气体和B气体在一定条件下在一密闭容器中发生如下反应:A(g)+3B(g)?2C(g)△H<0
有A气体和B气体在一定条件下在一密闭容器中发生如下反应:A(g)+3B(g)?2C(g)△H<0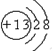 ,由A和B形成的含有非极性键的离子化合物的电子式是
,由A和B形成的含有非极性键的离子化合物的电子式是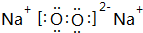 ;
;