题目内容
【题目】肉桂酸甲酯在医药工业中可作为有机合成的中间体,其中一种合成路线如下:

已知:①烃A是最简单的烯烃
②醛与醛能在一定条件下反应,原理如下:

回答下列问题:
(1)烃A的结构简式为____________。
(2)反应③的试剂和反应条件为___________;反应⑩的试剂和反应条件为______________;反应⑧的反应试剂______________(填“能”或“不能”)改用酸性高锰酸钾溶液,其原因是___________________。
(3)反应⑦的反应类型为______。
(4)H与银氨溶液反应的化学方程式为______________________。
(5)符合下列条件的I的同分异构体共有______种。
①除苯环外不含有其他环状结构;②能发生水解反应和银镜反应。
其中核磁共振氢谱显示为5组峰,且峰面积比为1:1:2:2:2的是______(写结构简式)
【答案】CH2=CH2氯气、光照CH3OH、浓H2SO4、加热不能碳碳双键被酸性高锰酸钾溶液氧化消去反应![]() 5
5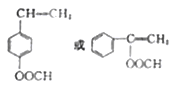
【解析】烃A为最简单的烯烃,故A为乙烯,与水发生加成反应生成B为乙醇,B发生氧化反应生成C为CH3CHO.乙醛与F发生信息中反应得到G,故F中含有醛基,结合转化关系可知,甲苯与氯气发生甲基上的取代反应生成D为![]() ,D发生发生水解反应生成E为
,D发生发生水解反应生成E为![]() ,E发生氧化反应生成F为
,E发生氧化反应生成F为![]() ,结合信息可知,G为
,结合信息可知,G为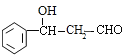 ,H为
,H为![]() ,I为
,I为![]() ,I与甲醇反应生成肉桂酸甲酯为
,I与甲醇反应生成肉桂酸甲酯为![]() ;
;
(1)乙烯的结构简式为CH2=CH2;
(2)反应③是甲苯与氯气发生甲基上的取代反应生成![]() ,同反应条件为氯气、光照 ;反应⑩是
,同反应条件为氯气、光照 ;反应⑩是![]() 与甲醇发生酯化反应生成肉桂酸甲酯为
与甲醇发生酯化反应生成肉桂酸甲酯为![]() ,所需试剂和反应条件为CH3OH、浓H2SO4并 加热;因酸性高锰酸钾溶液有强氧化性,能氧化碳碳双键,则反应⑧的试剂不能改用酸性高锰酸钾溶液;
,所需试剂和反应条件为CH3OH、浓H2SO4并 加热;因酸性高锰酸钾溶液有强氧化性,能氧化碳碳双键,则反应⑧的试剂不能改用酸性高锰酸钾溶液;
(3)反应⑦是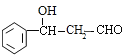 发生消去反应生成;
发生消去反应生成;
(4)![]() 与银氨溶液反应的化学方程式为
与银氨溶液反应的化学方程式为![]() ;
;
(5)①除苯环外不含有其他环状结构;②能发生水解反应和银镜反应说明存在酯基,可能是甲酸酯,即可能含有HCOO—和—CH=CH2,苯环上如果有两个取代基,应该是对位、邻位及间位共3种,另外苯环上可能只有一个取代基,应该有2种,共5种,其中核磁共振氢谱显示为5组峰,且峰面积比为1:1:2:2:2的是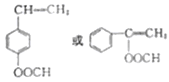 。
。

 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案【题目】下表列出了周期表中前20号元素中的十种元素的相关数据:
元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
原子半径(10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
最高价态 | +1 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | — |
最低价态 | — | — | -2 | — | -4 | -3 | -1 | — | -3 | -1 |
试回答下列问题:
(1)以上10种元素的原子中,最容易失去电子的是________(填元素编号),其最高价氧化物的水化物的电子式为___________;与H2最容易化合的非金属单质是________(写物质名称)。
(2)写出元素③形成的一种具有强氧化性的氢化物的结构式______________。
(3)写出上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的分子式______________;⑤的最高价氧化物的电子式为__________。
(4)短周期另一元素Q的原子半径为1.02×10-10m,则该元素在周期表中位于________________。
(5)写出④的最高价氧化物的水化物与⑦的最高价氧化物的水化物反应的离子方程式:________________________________________________________。
【题目】用下图所示实验装置进行实验研究(图中a、b、c表示止水夹),请对其方案进行完善或评价。
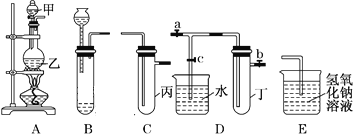
(1)实验室用装置A来制取Cl2,反应的离子方程式是______________;若将装置B、C、E相连后,用浓盐酸和______(填下列试剂的标号)为原料可制取Cl2。
a.KMnO4固体 b.KClO3固体 c.KCl固体 d.浓硫酸
(2)用装置B来制取制取氯气,并将装置B、C、E相连,在丙中加入适量水,即可制得氯水。向该氯水中加入大理石,充分振荡,观察到氯水的黄绿色逐渐褪去,同时产生少量气泡。某同学根据此现象推断出氯水呈酸性,请问该同学的推断是否合理?______________(填“合理”或“不合理”),若不合理,请说明理由(若合理,此空无需填写):_________________。
(3)为了探究氯水与大理石的反应,用装置A来制取氯气,并依次连接装置A、C、C、E。在第一个装置C的丙中,应加入的试剂是____________;在第二个装置C的丙中,加入适量水,即制得氯水。向制得的氯水中加入过量的大理石,反应结束后将所得溶液分成四等分,进行I、Ⅱ、Ⅲ、Ⅳ四个实验,实验操作如下,将实验现象或者实验结论填入下表:
实验序号 | 实验操作 | 实验现象 | 实验结论 |
Ⅰ | 将该溶液滴在有色布条上 | 有色布条迅速褪色 | ①该溶液中含有__________ |
Ⅱ | 向该溶液中滴加碳酸钠溶液 | ②___________ | 该溶液中含有Ca2+ |
Ⅲ | 向该溶液中滴加稀盐酸 | 有无色气泡产生 | ③无色气体是____________ |
Ⅳ | 加热该溶液 | 溶液变浑浊并产生大量气体 | ④该溶液中含有__________ |
⑤通过上述实验,得出氯水和过量的大理石反应的化学方程式为________________。
