题目内容
【题目】I.甲元素的原子序数是19,乙元素原子核外有两个电子层,最外电子层上有6个电子;丙是短周期元素中金属性最强的元素。由此推断:
(1)甲元素在周期表中位于第________周期;乙元素在周期表中位于第______族;丙元素的名称为________,丙的原子结构示意图为__________。
(2)甲的单质与水反应的离子方程式为________________;
乙单质与丙单质加热反应的化学方程式为________________。
II.最新报道,我国科学家通过与多个国家进行科技合作,成功研发出铯(Cs)原子喷泉钟,使我国时间频率基准的精度从30万年不差1秒提高到600万年不差1秒,标志着我国时间频率基准研究进入世界先进行列。已知铯位于元素周期表中第六周期第ⅠA族,根据铯在元素周期表中的位置,推断下列内容:
(1)铯的原子核外共有_________层电子,最外层电子数为_________,铯的原子序数为________。
(2)铯单质与水剧烈反应,放出________色气体,同时使紫色石蕊试液显________色,因为________________(写出化学方程式)。
(3)预测铯单质的还原性比钠单质的还原性________(填“弱”或“强”)。
【答案】 四 ⅥA 钠 略 2K+2H2O===2K++2OH-+H2↑ 2Na+O2Na2O2 6 1 55 无 蓝 2Cs+2H2O===2CsOH+H2↑ 强
【解析】I.甲元素的原子序数是19,因此甲是K;乙元素原子核外有两个电子层,最外电子层上有6个电子,所以乙是O;丙是短周期元素中金属性最强的元素,则丙是Na。
(1)K元素在周期表中位于第四周期;氧元素在周期表中位于第ⅥA族;丙元素的名称钠,Na的原子结构示意图为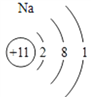 。(2)甲的单质与水反应的离子方程式为2K+2H2O=2K++2OH-+H2↑;乙单质与丙单质加热反应的化学方程式为2Na+O2
。(2)甲的单质与水反应的离子方程式为2K+2H2O=2K++2OH-+H2↑;乙单质与丙单质加热反应的化学方程式为2Na+O2![]() Na2O2。
Na2O2。
II.(1)已知铯位于元素周期表中第六周期第ⅠA族,所以铯的原子核外共有6层电子,最外层电子数为1,铯的原子序数为55。(2)铯单质与水剧烈反应,放出无色色气体氢气,同时生成强碱氢氧化铯,使紫色石蕊试液显蓝色,反应的化学方程式为2Cs+2H2O=2CsOH+H2↑。(3)同主族自上而下金属性逐渐增强,则铯单质的还原性比钠单质的还原性强。

【题目】【2016上海卷】随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点。
完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
已知H2的体积分数随温度升高而增加。
若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”或“不变”)
v正 | v逆 | 平衡常数K | 转化率α |
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[CO2]/mol·L-1 | [H2]/mol·L-1 | [CH4]/mol·L-1 | [H2O]/mol·L-1 | |
平衡Ⅰ | a | b | c | d |
平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为_________。
(3)碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11
草酸:H
0.1 mol/L Na2CO3溶液的pH____________0.1 mol/L Na2C2O4溶液的pH。(选填“大于”、“小于”或“等于”)
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是___________。
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____。(选填编号)
a.[H+]>[HC2O4-]>[HCO3-]>[CO32-]
B.[HCO3-]>[HC2O4-]>[C2O42-]>[CO32-]
c.[H+]>[HC2O4-]>[C2O42-]>[CO32-]
D.[H2CO3] >[HCO3-]>[HC2O4-]>[CO32-]
(4)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3-![]() H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。_______________________
H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。_______________________



