��Ŀ����
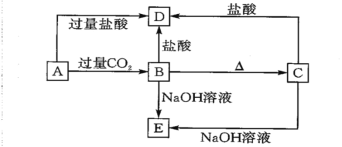
����Ŀ�������(Li2O)��﮵�ع�ҵ����Ҫԭ�ϡ��Դ�̼���Ϊԭ���Ʊ�����﮵�һ�ֹ����������£�

ע�������£�̼�������ˮ��������﮿�����ˮ��
��1����Ӧ����ͨ��CO2���ѹ��ԭ����______��
��2���ٷ�Ӧ������LiOH�Ļ�ѧ����ʽΪ______��
��ʯ����Ĺ�Һ��[Ca(OH)2��������H2O�����֮��]��LiOH���ʺ���Һ��LiOHŨ�ȵ�Ӱ������ͼ��ʾ��ʵ��������ѡ���Һ��25 g��L-1������Һ�ȹ��ͶԺ��������IJ���Ӱ����______��

��3��Ũ�����ᾧ����LiOH��H2Oͨ�����յõ�Li2O��
��LiOH��H2O�г�����������Li2CO3���������ʶ�����Li2O�ô�����Ӱ�죬��ԭ����______��
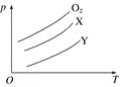
�ڽ�LiOH��H2O���ڲ�ͬ�����ڣ��ڿ����г�����գ���Ӧ���������XRDͼ������ͼ��ʾ��XRDͼ�������ж�ij��̬�����Ƿ���ڣ���ͬ��̬���ʳ�������������Dz�ͬ�������Ƶøߴ�����������˵�������______���������з�����Ӧ�Ļ�ѧ����ʽΪ______��

���𰸡� �ٽ�Li2CO3��ת�����ӿ�Li2CO3��Ӧ������ LiHCO3��Ca(OH)2��CaCO3��LiOH��H2O ������ҺLiOHŨ��̫�ͣ������ں��ڵ�Ũ���ᾧ Li2CO3���·ֽ�����Li2O ﮻��������� 20LiOH��H2O��4Fe��3O2![]() 4Li5FeO4��30H2O
4Li5FeO4��30H2O
��������(1)��Ӧ����̼�������Һ�������̼��Ӧ����LiHCO3��ͨ��CO2ʱ����ѹ���Դٽ�Li2CO3��ת�����ӿ�Li2CO3��Ӧ�����ʣ��ʴ�Ϊ���ٽ�Li2CO3��ת�����ӿ�Li2CO3��Ӧ��������
(2)�ٷ�Ӧ������Һ��ʯ���鷴Ӧ����LiOH����Ӧ�Ļ�ѧ����ʽΪLiHCO3��Ca(OH)2��CaCO3��LiOH��H2O���ʴ�Ϊ��LiHCO3��Ca(OH)2��CaCO3��LiOH��H2O��
�ڸ���ʯ����Ĺ�Һ��[Ca(OH)2��������H2O�����֮��]��LiOH���ʺ���Һ��LiOHŨ�ȵ�Ӱ���֪��ʵ��������ѡ���Һ��25 g��L-1������Һ�ȹ�����������ҺLiOHŨ��̫�ͣ������ں��ڵ�Ũ���ᾧ���ʴ�Ϊ��������ҺLiOHŨ��̫�ͣ������ں��ڵ�Ũ���ᾧ��
(3)��LiOH��H2O�г�����������Li2CO3���������ʶ�����Li2O�ô�����Ӱ�죬����ΪLi2CO3�������ֽ�����Li2O�Ͷ�����̼���ʴ�Ϊ��Li2CO3���·ֽ�����Li2O��
(3)Ũ�����ᾧ����LiOH��H2Oͨ�����յõ�Li2O��
�ڽ�LiOH��H2O���ڲ�ͬ�����ڣ��ڿ����г�����գ����ݷ�Ӧ���������XRDͼ��֪�����Ƶøߴ�����������˵�������﮻���������������������LiOH��H2O���ȷ�Ӧ�õ�Li5FeO4����Ӧ�ķ���ʽΪ20LiOH��H2O��4Fe��3O2![]() 4Li5FeO4��30H2O���ʴ�Ϊ��﮻�����������20LiOH��H2O��4Fe��3O2
4Li5FeO4��30H2O���ʴ�Ϊ��﮻�����������20LiOH��H2O��4Fe��3O2![]() 4Li5FeO4��30H2O��
4Li5FeO4��30H2O��