题目内容
【题目】某同学将 0.1mol/L 的 K2SO4 溶液 V 1 L 与 0 . 2 mo l / L 的 Al2(SO4)3溶液 V 2 L 混合,再加入 V 3 L 蒸馏水,假定溶液 总体积 V 总 =V1 +V 2 +V 3 .并测得混合液中三种离子物质的量浓度 分别为:K+:0 .1 mo l /L ,Al3+:0 .1 mo l /L,SO42-:0 . 2 mo l / L , 则 下 列 判 断 正 确 的 是( )
A. 一定是 2L K2SO4 溶液和 1L Al2(SO4)3溶液混合,再加 1L 蒸馏水
B. 混合液中K+浓度与Al3+浓度数值之和大于SO42-浓度数值
C. 三种液体体积比为 V1:V2:V3=2:1:1
D. 混合液中 K2SO4 物质的量等于 Al2(SO4)3物质的量的一半
【答案】C
【解析】
c(K+)=![]() ①
①
(Al3+)=![]() mol·L-1 ②
mol·L-1 ②
(SO42-)=![]() mol·L-1 ③
mol·L-1 ③
将①/②可求出V1/V2;从而求出V总,即可求出V1:V2:V3。
c(K+)=![]() ①
①
(Al3+)=![]() mol·L-1 ②
mol·L-1 ②
(SO42-)=![]() mol·L-1 ③
mol·L-1 ③
将①/②可求出V1/V2=2:1;设V1=2L,则V2=1L,带入③可得V总=4L,故V3=1L.即三种液体体积比为V1:V2:V3=2:1:1。
A、三种液体体积比为V1:V2:V3=2:1:1,故混合溶液可以是2L K2SO4溶液和1L Al2(SO4)3溶液混合,再加1L蒸馏水,但不一定,故A错误;
B、由于混合液中三种离子物质的量浓度分别为:K+:0.1mol·L-1,Al3+:0.1mol·L-1,SO42-:0.2mol·L-1,故K+浓度与Al3+浓度数值之和等于SO42-浓度数值,故B错误;
C、三种液体体积比为V1:V2:V3=2:1:1,故C正确;
D、混合液中K2SO4 物质的量与Al2(SO4)3的物质的量之比为:(0.1mol·L-1×2L):(0.2mol·L-1×1L)=1:1,故两者的物质的量相等,故D错误。
故选C。

【题目】硫和钙的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)基态Ca原子中,核外电子占据最高能层的符号是________,该能层为次外层时最多可以容纳的电子数为_________。元素Ca和S相比,第一电离能较大的是______(填元素符号)。
(2)钙元素的焰色反应呈砖红色,其中红色对应的辐射与钾元素的焰色反应对应颜色的辐射波长,较短的是_______(填元素符号)。
(3)H2S和H2O分子构型都为V形,中心原子的杂化形式都是______,但H2O分子键角大于H2S分子,原因是________________。
(4)钙元素和锰元素属于同一周期,且核外最外层电子构型相同,但金属钙的熔点、沸点等都比金属锰低,原因是________________。
(5)Ca、Mn、Mg的氧化物和硫化物都具是NaCl型结构的离子晶体,其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得它们的晶胞参数如下表:
氧化物晶体 | MgO | MnO | CaO |
a/nm | 0.421 | 0.444 | 0.480 |
硫化物晶体 | MgS | MnS | CaS |
a/nm | 0.520 | 0.520 | 0.568 |
由表可知:r(S2-)____r(O2-)(填“>”或“<”),r(Mg2+)、r(Ca2+)、r(Mn2+)由大到小的的顺序是__________,r(S2- )为_____nm,r(Ca2+)为_____nm。
【题目】钛与铁是很重要的金属。已成为化工生产中重要的材料。回答下列问题:
(1)基态钛原子的价电子排布式为__________________,金属钛晶胞如下左图所示,晶胞参数为a=b= 295.08pm,c=468.55pm,α=β=90%,y= 120%。金属钛为______________堆积(填堆积方式)。
(2)用熔融的镁在氩气中还原TiCl4可得到多空的海绵钛。已知TiCl4在通常情况下是无色液体,熔点为-23℃,沸点为136℃,可知TiCl4为____________晶 体。
(3)通过X-射线探明KCl、CaO、TiN晶体与NaCl晶体结构相似,且知两种离子晶体的晶格能数据如下:
离子晶体 | KCl | CaO |
晶格能(kJ/mol) | 715 | 3401 |
解释KCl晶格能小于CaO的原因:_______________。
钛可与C、N、O等元素形成二元化合物。C、N、O元素的电负性由大到小的顺序是________。
(4)钙钛矿晶体的结构如下右图所示。晶体的化学式为_________________。
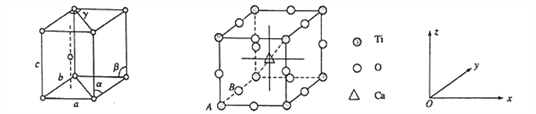
晶胞中的原子可用x、y、z组成的三数组来表达它在晶胞中的位置,称为原子坐标。已知原子坐标为A(0,0,0);B(0,1/2,0);则Ca 离子的原子坐标为______________。
(5)Fe有δ、γ、α三种同素异形体,其晶胞结构如下图所示:

①δ、α两种晶体晶胞中铁原子的配位数之比为_______________________。
②若Fe原子半径为rpm,NA表示阿伏加德罗常数的值,则δ-Fe单质的密度为________g/cm3(列出算式即可)。






