题目内容
醋酸是重要的一元酸,在有机和无机反应中都有应用。
(1)在酯化反应的实验中,乙酸、乙醇的用量和平衡时乙酸乙酯的生成量如下表:
反应 | 乙醇(mol) | 乙酸(mol) | 乙酸乙酯(mol) |
1 | 2 | 2 | 1.33 |
2 | 3 | 2 | 1.57 |
3 | 4 | 2 | x |
4 | 5 | 2 | 1.76 |
由表中数据推测,数值x的范围是________。
(2)现有25°C时,pH=3的醋酸。请回答以下问题:
①若向醋酸中加入少量醋酸钠固体,此时溶液中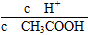 将________(填“增大”“减小”或“不变”);
将________(填“增大”“减小”或“不变”);
②若向醋酸中加入稀NaOH溶液,使其恰好完全反应,所得溶液的pH________7(填“>”“<”或“=”);
③若向醋酸中加入pH=11的NaOH溶液,且二者的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是________。
(1)1.57<x<1.76 (2)①减小 ②>
③c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
【解析】(1)根据表中数据,增大乙醇的量,平衡一定正向移动,生成乙酸乙酯的量一定增大。(2)①CH3COOH CH3COO-+H+,外加CH3COONa,c(CH3COO-)增大,平衡逆向移动,c(CH3COOH)增大,c(H+)减小,则
CH3COO-+H+,外加CH3COONa,c(CH3COO-)增大,平衡逆向移动,c(CH3COOH)增大,c(H+)减小,则 减小;②CH3COOH+NaOH=CH3COONa+H2O,二者完全反应后溶液中的溶质只有CH3COONa,CH3COONa可发生水【解析】
减小;②CH3COOH+NaOH=CH3COONa+H2O,二者完全反应后溶液中的溶质只有CH3COONa,CH3COONa可发生水【解析】
CH3COO-+H2O CH3COOH+OH-,c(OH-)>c(H+),溶液呈碱性;③CH3COOH是弱电解质,与NaOH反应后,CH3COOH过量,溶液呈酸性,所以c(CH3COO-)>c(Na+)>c(H+)>c(OH-)。
CH3COOH+OH-,c(OH-)>c(H+),溶液呈碱性;③CH3COOH是弱电解质,与NaOH反应后,CH3COOH过量,溶液呈酸性,所以c(CH3COO-)>c(Na+)>c(H+)>c(OH-)。

某兴趣小组为探究外界条件对可逆反应A(g)+B(g)  C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10 L的密闭容器中充入1 mol A和1 mol B,反应达平衡时测得容器中各物质的浓度为I。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ。
C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10 L的密闭容器中充入1 mol A和1 mol B,反应达平衡时测得容器中各物质的浓度为I。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ。
| A | B | C |
Ⅰ | 0.050 mol·L-1 | 0.050 mol·L-1 | 0.050 mol·L-1 |
Ⅱ | 0.070 mol·L-1 | 0.070 mol·L-1 | 0.098 mol·L-1 |
Ⅲ | 0.060 mol·L-1 | 0.060 mol·L-1 | 0.040 mol·L-1 |
Ⅳ | 0.080 mol·L-1 | 0.080 mol·L-1 | 0.12 mol·L-1 |
针对上述系列试验,下列结论中错误的是( )
A.由Ⅰ中数据可计算出该温度下反应的平衡常数K=20 mol-1·L
B.Ⅱ可能是通过增大C的浓度实现的
C.若Ⅲ只是升高温度,则与I比较,可以判断出正反应一定是放热反应
D.第Ⅳ组实验数据的得出,通过压缩容器的体积就可以实现