题目内容
【题目】若用AG表示溶液的酸度,其表达式为:![]() 。室温下,实验室里用0.1mol/L的盐酸溶液滴定10mL 0.1mol/L MOH溶液,滴定曲线如下图所示。下列说法正确的是
。室温下,实验室里用0.1mol/L的盐酸溶液滴定10mL 0.1mol/L MOH溶液,滴定曲线如下图所示。下列说法正确的是
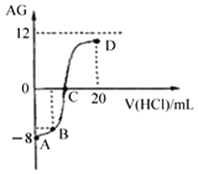
A. 该滴定过程可选择酚酞作为指示剂
B. C点时加入盐酸溶液的体积等于10 mL
C. 溶液中由水电离的c(H+):C点>D点
D. 若B点加入的盐酸溶液体积为5 mL,所得溶液中:c(M+)+c(H+)= c(MOH)+ c(OH-)
【答案】C
【解析】A.用0.1mol/L的盐酸溶液滴定10mL 0.1mol/L MOH溶液,AG=-8,AG=lg[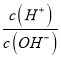 ],
], 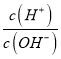 =10-8,c(H+)c(OH-)=10-14,c(OH-)=10-3mol/L,说明MOH为弱碱,恰好反应溶液显酸性,选择甲基橙判断反应终点,故A错误;B.C点是AG=0,c(H+)=c(OH-)=10-7,溶液呈中性,溶质为MCl和MOH混合溶液,C点时加入盐酸溶液的体积小于10 mL,故B错误;C.滴定过程中从A点到D点溶液中水的电离程度,A-B滴入盐酸溶液中氢氧根离子浓度减小,对水抑制程度减小,到恰好反应MCl,M+离子水解促进水电离,电离程度最大,继续加入盐酸抑制水电离,滴定过程中从A点到D点溶液中水的电离程度,D<A<B<C,故C正确; D.若B点加入的盐酸溶液体积为5 mL,得到等浓度的MCl和MOH混合溶液,溶液中存在电荷守恒c(M+)+c(H+)=c(OH-)+c(Cl-),物料守恒为:c(M+)+c(MOH)=c(Cl-),消去氯离子得到:c(M+)+2c(H+)=c(MOH)+2c(OH-),故D错误;故选C。
=10-8,c(H+)c(OH-)=10-14,c(OH-)=10-3mol/L,说明MOH为弱碱,恰好反应溶液显酸性,选择甲基橙判断反应终点,故A错误;B.C点是AG=0,c(H+)=c(OH-)=10-7,溶液呈中性,溶质为MCl和MOH混合溶液,C点时加入盐酸溶液的体积小于10 mL,故B错误;C.滴定过程中从A点到D点溶液中水的电离程度,A-B滴入盐酸溶液中氢氧根离子浓度减小,对水抑制程度减小,到恰好反应MCl,M+离子水解促进水电离,电离程度最大,继续加入盐酸抑制水电离,滴定过程中从A点到D点溶液中水的电离程度,D<A<B<C,故C正确; D.若B点加入的盐酸溶液体积为5 mL,得到等浓度的MCl和MOH混合溶液,溶液中存在电荷守恒c(M+)+c(H+)=c(OH-)+c(Cl-),物料守恒为:c(M+)+c(MOH)=c(Cl-),消去氯离子得到:c(M+)+2c(H+)=c(MOH)+2c(OH-),故D错误;故选C。

 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案【题目】将牛奶和姜汁混合,待牛奶凝固便成为一种富有广东特色的甜品——姜撞奶。为了掌握牛奶凝固所需的条件,某同学在不同温度的等量牛奶中混人一些新鲜姜汁,观察混合物15min,看其是否会凝固,结果如下表。请回答下列问题:
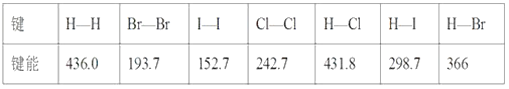
温度(℃) | 20 | 40 | 60 | 80 | 100 |
结果 | 15min后仍未有凝固迹象 | 14min内完全凝固 | 1min内完全凝固 | 1min内完全凝固 | 15min后仍未有凝固迹象 |
(注:用曾煮沸的姜汁重复这项实验,牛奶在任何温度下均不能凝固)
(1)实验证明新鲜姜汁中含有一种酶,其作用是 。
(2)20℃和100℃时,15min后仍未有凝固迹象,说明酶的活性较低,其原因分别是 和 。
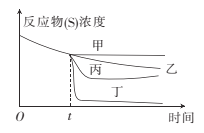
(3)若60℃时牛奶在有姜汁和没有姜汁的情况下都可以凝固,当反应进行到t时,向其中加人姜汁。下图中能正确表示加姜汁后牛奶凝固随时间变化趋势的曲线是 。
(4)为提高实验的准确度,实验中“不同温度的等量牛奶中混入一些新鲜姜汁”操作中应注意的是 。
(5)有同学说,该实验不能得出姜汁使牛奶凝固的最适温度,请提出解决方案: 。