题目内容
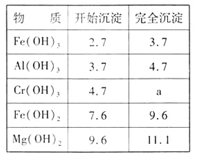
(9分) 现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图,

请计算出(1)a处沉淀的总物质的量 mol;
(2)c(FeCl3)= mol/L ; (3)c(AlCl3)= mol/L

请计算出(1)a处沉淀的总物质的量 mol;
(2)c(FeCl3)= mol/L ; (3)c(AlCl3)= mol/L
(1)1 (2) 4 (3) 6
氯化铁、氯化铝和氢氧化钠反应分别生成氢氧化铁和氢氧化铝沉淀。但氢氧化铝是两性氢氧化物,能溶于氢氧化钠中。所以根据图像可知a点是氢氧化铁和氢氧化铝沉淀,b点是氢氧化铁沉淀。溶解氢氧化铝消耗氢氧化钠是0.6mol。所以根据方程式Al(OH)3+NaOH=NaAlO2+2H2O可知氢氧化铝是0.6mol,根据原子守恒可知氯化铝也是0.6mol,浓度是0.6mol÷0.1L=6.0mol/L。根据反应FeCl3+3NaOH=Fe(OH)3↓+3NaCl、AlCl3+3NaOH=Al(OH)3↓+3NaCl可知,生成0.6mol氢氧化铝消耗氢氧化钠是1.8mol,所以和氯化铁反应的氢氧化钠是3mol-1.8mol=1.2mol,因此氯化铁是0.4mol,浓度是4.0mol/L。氢氧化铁和氢氧化铝一共是0.6mol+0.4mol=1.0mol。

练习册系列答案
相关题目
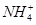 + [AI(OH)4]— ===
+ [AI(OH)4]— ===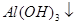
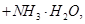 向含有等物质的量的
向含有等物质的量的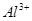 、
、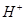 的混合溶液中,慢慢滴加NaOH溶液,直至过量,发生以下离子反应:
的混合溶液中,慢慢滴加NaOH溶液,直至过量,发生以下离子反应: 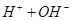 ===
===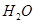 ②
②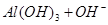 ===[AI(OH)4]—③
===[AI(OH)4]—③ ===
===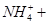
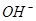 ===
===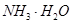 发生反应的先后顺序正确的是
发生反应的先后顺序正确的是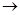 ④
④