题目内容
(5分)氯酸钾与浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,反应的化学方程式为:2KClO3 + 4HCl(浓) === 2KCl + 2ClO2↑+ Cl2↑+ 2H2O
(1)用双线桥表示上述反应中电子转移的方向和数目。
(2)浓盐酸在该反应中表现的性质是________(填序号)。
① 只有还原性 ② 还原性和酸性 ③ 只有氧化性 ④ 氧化性和酸性
(3)上述反应产生0.2 mol Cl2时,转移的电子数约为______________。
(1)用双线桥表示上述反应中电子转移的方向和数目。
(2)浓盐酸在该反应中表现的性质是________(填序号)。
① 只有还原性 ② 还原性和酸性 ③ 只有氧化性 ④ 氧化性和酸性
(3)上述反应产生0.2 mol Cl2时,转移的电子数约为______________。
(5分)
(1)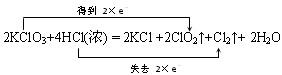 (2分,若写成2e-也得分)
(2分,若写成2e-也得分)
(2)② (2分)
(3)2.408×1023 (1分)
(1)
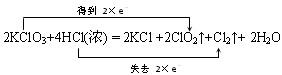 (2分,若写成2e-也得分)
(2分,若写成2e-也得分)(2)② (2分)
(3)2.408×1023 (1分)
(2)浓盐酸在反应中部分氯失电子生成氯气,表现还原性,部分转变为氯化钾,表现酸性
(3)由(1)可知,当产生0.2 mol Cl2时,反应有0.4 mol e—转移,
(3)由(1)可知,当产生0.2 mol Cl2时,反应有0.4 mol e—转移,

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
 +2FeS+SO2,(方程式已配平)
+2FeS+SO2,(方程式已配平) 8MnSO4+9K2SO4+40CO2↑+32H2O
8MnSO4+9K2SO4+40CO2↑+32H2O g KMnO4与12mol/L的浓HCl发生。反应方程式如下:2KMnO4+ 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O 通过计算解答以下问题:
g KMnO4与12mol/L的浓HCl发生。反应方程式如下:2KMnO4+ 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O 通过计算解答以下问题: