题目内容
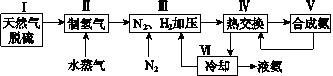
【题目】合成氨是人类科学技术上的一项重大突破,其反应原理为N2(g)+3H2(g)![]() 2NH3(g)ΔH=-92.4kJ·mol-1。一种工业合成氨的简式流程图如下:
2NH3(g)ΔH=-92.4kJ·mol-1。一种工业合成氨的简式流程图如下:
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:_______________________。
(2)步骤Ⅱ中制氢气的原理如下:
①CH4(g)+H2O(g)![]() CO(g)+3H2(g)△H=+206.4kJ·mol-1
CO(g)+3H2(g)△H=+206.4kJ·mol-1
②CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=-41.2kJ·mol-1
CO2(g)+H2(g)△H=-41.2kJ·mol-1
对于反应①,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是____________。
a.升高温度b.增大水蒸气浓度c.加入催化剂d.降低压强
利用反应②,将CO进一步转化,可提高H2的产量。若1molCO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18molCO、CO2和H2的混合气体,则CO的转化率为__________。
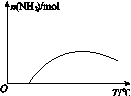
(3)图(a)表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:____________。
(4)依据温度对合成氨反应的影响,在图(b)坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。


(a)(b)
(5)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)________。简述本流程中提高合成氨原料总转化率的方法:______________________________。
【答案】(1)2NH4HS+O2=2NH3·H2O+2S↓(2)a90%
(3)14.5%
(4)如下图
(5)Ⅳ对原料气加压;分离液氨后,未反应的N2、H2循环使用
【解析】
试题分析:(1)H2S杂质常用氨水吸收,产物为NH4HS,一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,说明又生成一水合氨,化学方程式为:2NH4HS+O2=2S↓+2NH3H2O;
(2)对于反应①正反应为气体体积增大吸热反应;a.反应是吸热反应,升高温度,反应速率增大,平衡正向进行,平衡体系中H2百分含量增大,故a符合;b.增大水蒸气浓度,平衡正向进行,反应速率增大,但平衡体系中H2百分含量不一定增大,故b不符合;c.加入催化剂,改变反应速率不改变化学平衡,反应速率增大,氢气百分含量不变,故c不符合;d.降低压强,反应速率减小,平衡逆向进行,氢气百分含量减小,故d不符合;若1molCO和H2的混合气体(CO的体积分数为20%)中CO为0.2mol,H2的物质的量为0.8mol,与H2O反应,得到1.18molCO、CO2和H2的混合气体,设转化的一氧化碳的物质的量为x,则:
CO(g)+H2O(g)CO2(g)+H2(g)
起始量(mol)0.200.8
变化量(mol)xxx
平衡量(mol)0.2-xxx+0.8
则0.2-x+x+x+0.8=1.18,解得x=0.18,则CO转化率为0.18mol/0.2mol×100%=90%;
(3)a点氮气的体积分数为42%,氢气与氮气物质的量之比为3:1,二者按3:1反应,平衡时二者体积分数之比为3:1,则平衡时氮气体积分数为(1-42%)×1/4=14.5%;
(4)随反应进行氨气物质的量增大,达到平衡状态,合成氨的反应是放热反应,继续升温,平衡逆向进行,氨气物质的量减小,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图为: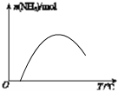 ;
;
(5)合成氨为放热过程,通过Ⅳ热交换器加热反应混合气体,使反应达到所需温度,使合成氨放出的能量得到充分利用;将氨气液化,分离出氨气促进平衡正向进行,把平衡混合气体中氮气和氢气重新循环使用,提高原理利用率。