题目内容
15.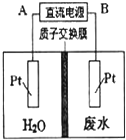 用如图所示装置处理含 NO${\;}_{3}^{-}$的酸性工业废水,某电极反应式为 2NO${\;}_{3}^{-}$+12H++10e-═N2↑+6H2O,请回答下列问题.
用如图所示装置处理含 NO${\;}_{3}^{-}$的酸性工业废水,某电极反应式为 2NO${\;}_{3}^{-}$+12H++10e-═N2↑+6H2O,请回答下列问题. (1)电源正极为A( 填“A”或“B”),与该电极连接的Pt电极反应式为4OH?-4e?═2H2O+O2↑.
(2)电解时 H+从质子交换膜侧向侧移动右( 填“左”或“右”).
(3)电解过程中,左侧电解液pH减小( 填“增大”“减小”或“不变”).
(4)电解池一侧生5.6gN2,另一侧溶液质量减少18g.
( 5 )若上述直流电源采用乙醇燃料电池,电解质溶液为KOH溶液,通入氧气的电极为正极( 填“正极”或“负极”),写出负极的电极反应式CH3CH2OH-12e-+16OH-═2CO32-+11H2O.
分析 据电极反应式为2NO3-+12H++10e-=N2+6H2O,可知,该反应为还原反应,为阴极反应式,废水在右边反应,说明右边阴极;左边阳极,氢氧根离子在阳极放电生成氧气和氢离子,据电子守恒和原子守恒解答.
解答 解:据电极反应式为2NO3-+12H++10e-=N2+6H2O,可知,该反应为还原反应,为阴极反应式,废水在右边反应,说明右边阴极;左边阳极,氢氧根离子在阳极放电生成氧气和氢离子,
(1)根据以上分析,左边阳极,所以电源正极为A,反应为4OH?-4e?═2H2O+O2↑,故答案为:A;4OH?-4e?═2H2O+O2↑;
(2)电解时 H+从质子交换膜侧移向阴极即从左到右,故答案为:左;右;
(3)电解过程中,左边阳极,反应为4OH?-4e?═2H2O+O2↑,所以左侧电解液pH减小,故答案为:减小;
(4)根据电子守恒,电解池一侧生5.6gN2,2NO3-+12H++10e-=N2+6H2O则转移$\frac{5.6}{28}$×10=2mol,另一侧即右侧反应为4OH?-4e?═2H2O+O2↑,每有2mol水电解转移4mol电子,则阳极被电解的水的质量为1mol×18g/mol=18g,故答案为:18g;
( 5 )乙醇燃料电池,电解质溶液为KOH溶液,通入氧气的电极为正极,负极为乙醇失电子发生氧化反应,反应式为:CH3CH2OH-12e-+16OH-═2CO32-+11H2O;故答案为:正极;CH3CH2OH-12e-+16OH-═2CO32-+11H2O.
点评 本题考查了电解原理的应用,注意电子守恒和阳极发生氧化反应阴极发生还原反应,题目难度中等.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
6.某物质的水溶液能导电,且溶液中不存在溶质分子,但该物质属于非电解质,符合该条件的物质是( )
| A. | Cl2 | B. | CO2 | C. | NO2 | D. | NaCl |
3.某小组为研究电化学原理,设计如图装置.下列叙述正确的是( )


| A. | a和b不连接时,铁片、铜片上均无反应发生 | |
| B. | a和b用导线连接时,溶液中Cu2+向铁电极移动 | |
| C. | a和b分别连接直流电源正、负极,铜电极质量减少 | |
| D. | a和b分别连接直流电源正、负极,溶液中Cu2+向铜电极移动 |
20.下列事实与胶体性质无关的是( )
| A. | “尿毒症”患者做血液透析治疗 | |
| B. | 在河流入海处易形成沙洲 | |
| C. | 在豆浆里加入盐卤做豆腐 | |
| D. | 三氯化铁溶液中滴入氢氧化钠液出现红褐色沉淀 |
7.下列物质加入水中,因水解而使溶液呈酸性的是( )
| A. | CuCl2 | B. | NaHSO4 | C. | NaHCO3 | D. | SO2 |
5.下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为( )
| A. | 蒸馏水 氨水 氧化铝 二氧化硫 | |
| B. | 盐酸 空气 硫酸 干冰 | |
| C. | 胆矾 盐酸 铁 碳酸钙 | |
| D. | 生石灰 硫酸 氯化铜 碳酸钠 |
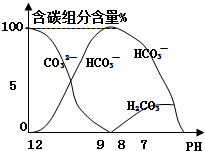 常温下在10mL0.1mol•L-1 Na2CO3溶液中逐滴加入0.1mol•L-1 HCl溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液PH变化的部分情况如图所示.根据图示回答下列问题:
常温下在10mL0.1mol•L-1 Na2CO3溶液中逐滴加入0.1mol•L-1 HCl溶液20mL,溶液中含碳元素的各种微粒的质量分数(纵轴)随溶液PH变化的部分情况如图所示.根据图示回答下列问题: