题目内容
【题目】已知:1molH2(g)与1molBr2(g)完全反应生成2molHBr(g)时放出72kJ的热量,有关物质的相关数据如下表:
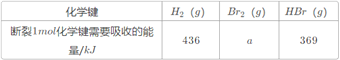
则表中a为( )
A. 404 B. 260 C. 230 D. 200
【答案】C
【解析】根据盖斯定律计算反应H2(g)+Br2(g)=2HBr(g)的△H,结合反应热等于反应物的总键能减生成物的总键能列方程计算。
1mol H2(g)与1mol Br2(g)完全反应生成2mol HBr(g)时放出72kJ的热量,即热化学方程式为H2(g)+Br2(g)=2HBr(g)△H=-72kJ/mol反应中,反应热等于反应物的总键能减生成物的总键能,则-72=436+a-2×369,解得a=230,答案选C。

练习册系列答案
相关题目