题目内容
【题目】用含少量镁的铝粉制取纯净的Al(OH)3,下列操作步骤可行的组合是
①加盐酸溶解 ②加烧碱溶液溶解 ③过滤 ④通入足量二氧化碳 ⑤加过量烧碱溶液 ⑥加过量盐酸
A.②③④③B.①⑤④③C.①⑤③⑥③D.①⑤⑥③
【答案】A
【解析】
镁、铝都能与酸反应,但铝可溶于强碱,所以可加入烧碱溶液溶解,过滤后可到NaAlO2溶液,在反应后的溶液中加入弱酸,可通入过量CO2,生成Al(OH)3沉淀,经过滤、洗涤可得到纯净的氢氧化铝,正确顺序为②③④③,答案选A。

【题目】实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为:
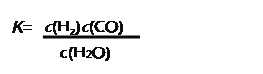 它所对应的化学反应为:__________
它所对应的化学反应为:__________
(2)已知在400℃时,N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正_____v(N2)逆(填:>、<、=、不能确定);欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积分数增加,
2NH3(g) ΔH<0的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正_____v(N2)逆(填:>、<、=、不能确定);欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积分数增加,
可采取的正确措施是____________(填序号)
A. 缩小体积增大压强 B.升高温度 C.加催化剂 D.使氨气液化移走
(3)在一定体积的密闭容器中,进行如下化学反应:
A(g)+3B(g) ![]() 2C(g)+D(s) ΔH,其化学平衡常数K与温度t的关系如下表:
2C(g)+D(s) ΔH,其化学平衡常数K与温度t的关系如下表:
t/K | 300 | 400 | 500 | …… |
K/(mol·L-1)2 | 4×106 | 8×107 | K1 | …… |
请完成下列问题:
①判断该反应的ΔH _______0(填“>”或“<”)
②在一定条件下,能判断该反应一定达化学平衡状态的是________ (填序号)。
A. 3v(B)(正)=2v(C)(逆) B.容器内压强保持不变
C.A和B的转化率相等 D.混合气体的密度保持不变
