题目内容
【题目】化合物X是一种黄酮类化合物的中间体,其结构简式如图所示。下列有关化合物X的说法正确的是

A. 该有机物分子式为C24H22O5
B. 能发生取代反应、加成反应和氧化反应
C. 1mol化合物X最多能与2mol NaOH反应
D. 1mol化合物X最多可与11mol H2发生加成反应
【答案】BD
【解析】A. 该有机物分子式为C24H20O5,故A错误;B. X分子含有苯环氢原子、侧链烃基氢原子、酚羟基、酯基等,所以能发生取代反应,X分子含有不饱和结构苯环、羰基,所以能发生加成反应,X分子含有酚羟基、侧链甲基,所以能发生氧化反应,故B正确;C. X的酚羟基和酯基水解生成的羧基、酚羟基都能与氢氧化钠发生反应,所以1mol化合物X最多能与3molNaOH反应,故C错误;D. X的苯环、羰基都可与氢气发生加成反应,1mol化合物X最多可与11molH2发生加成反应,故D正确。故选BD。

【题目】氯气可用于制取漂白剂和自来水消毒。
(1)将氯气通入水中制得氯水,氯水可用于漂白,其中起漂白作用的物质是 __________(填写
化学式)。
(2)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶
液中,反应的离子方程式为__________。
(3)同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的pH=12;
步骤2:取稀释后溶液各20 mL分别加入3个洁净的小烧杯中;
步骤3:用硫酸将3个烧杯内溶液的pH分别调至10、7和4。(溶液体积变化忽略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
烧杯 | 溶液的pH | 现象 |
a | 10 | 10 min后,红纸基本不褪色;4h后红纸褪色 |
b | 7 | 10 min后,红纸颜色变浅;4 h后红纸褪色 |
c | 4 | 10 min后,红纸颜色变得更浅;4h后红纸褪色 |
已知,溶液中Cl2、HC1O和ClO-物质的量分数(α) 随pH变化的关系如右图所示:
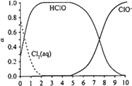
①由实验现象可获得以下结论:溶液的pH在4 ~10范围内,pH越大,红纸褪色________。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是________。
(4)由于氯气会与自来水中的有机物发生反应,生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如ClO2气体就是一种新型高效含氯消毒剂。
①一种制备ClO2的方法是将SO2通入硫酸酸化的NaC1O3溶液中,反应的离子方程式为__________。
②另一种制备ClO2的方法是用NaClO3与盐酸反应,同时有Cl2生成,产物中Cl2体积约占1/3。则每生成0.5 mol ClO2,转移__________mole-。