题目内容
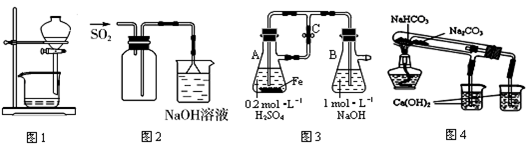
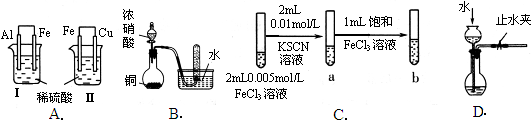
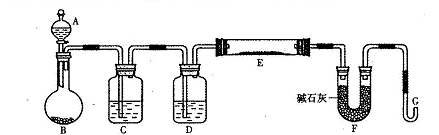
下述实验方案能达到实验目的的是
| 编号 | A | B | C | D |
| 实验 方案 |  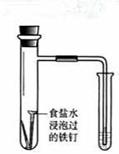 食盐水 | 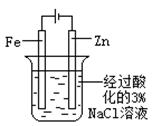 片刻后在Fe电极附近滴入K3[Fe(CN)6]溶液 | 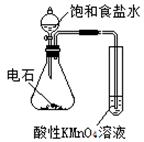 | 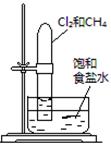 置于光亮处 |
| 实验 目的 | 验证铁钉发生 析氢腐蚀 | 验证Fe电极被保护 | 验证乙炔的还原性 | 验证甲烷与氯气发生 化学反应 |
D
试题分析:A、析氢腐蚀是在酸性条件下发生的,在食盐水中发生吸氧腐蚀,错误;B、电解池阳极的金属被强烈腐蚀,无法被保护,错误;C、因为电石是混合物,与水反应时生成的乙炔气体中含有H2S气体,也具有还原性,也能使酸性高锰酸钾溶液褪色,所以必须除杂红眼才能通过酸性高锰酸钾溶液验证乙炔的还原性,错误;D、Cl2能溶于水,所以可以更加液面的变化验证甲烷与氯气的反应,正确。

练习册系列答案
相关题目

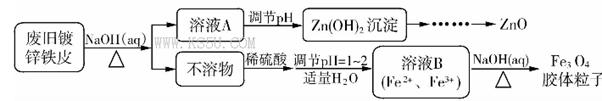
 Fe3O4(胶体)+S4O62-+H2O
Fe3O4(胶体)+S4O62-+H2O