题目内容
铁是人体必需的微量元素之一,医学上常用硫酸亚铁糖衣片(主要成分为FeSO4?7H2O)给贫血病人补铁,为测定该糖衣片中铁元素的含量,某实验小组做了如下实验:
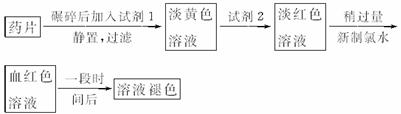
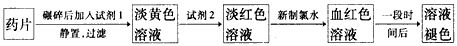
步骤一:取本品10片,称量,除去糖衣,研细,用新煮沸过的冷水溶解,过滤,将滤液配制成250mL溶液.
步骤二:取所配溶液25.00mL于锥形瓶中,使用酸性KMnO4,溶液滴定至终点.
步骤三:重复步骤一、步骤二.
三次滴定分别消耗0.0010mol/L KMnO4溶液21.44mL、21.43mL、21.42mL.
请回答下列问题:
(1)配制样品溶液时把水煮沸的原因是
(2)酸性KMnO4溶液与Fe2+反应的离子方程式
(3)上述实验中所用的KMO4溶液要进行酸化,用于酸化的酸是
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.三种都可以
(4)滴定前, (填仪器名称)应使用KMnO4溶液润洗,滴定时如何判断已经达到终点?
(5)由上述实验数据,计算每片硫酸亚铁糖衣片中含有铁元素为 mg.
步骤一:取本品10片,称量,除去糖衣,研细,用新煮沸过的冷水溶解,过滤,将滤液配制成250mL溶液.
步骤二:取所配溶液25.00mL于锥形瓶中,使用酸性KMnO4,溶液滴定至终点.
步骤三:重复步骤一、步骤二.
三次滴定分别消耗0.0010mol/L KMnO4溶液21.44mL、21.43mL、21.42mL.
请回答下列问题:
(1)配制样品溶液时把水煮沸的原因是
(2)酸性KMnO4溶液与Fe2+反应的离子方程式
(3)上述实验中所用的KMO4溶液要进行酸化,用于酸化的酸是
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.三种都可以
(4)滴定前,
(5)由上述实验数据,计算每片硫酸亚铁糖衣片中含有铁元素为
分析:(1)亚铁离子具有较强的还原性,容易被氧气氧化;
(2)酸性高锰酸钾具有强氧化性,将Fe2+氧化为Fe3+,被还原为Mn2+,同时生成水;
(3)用高锰酸钾溶液滴定,加入的酸不能具有氧化性,不能与高锰酸钾溶液反应;
(4)高锰酸钾溶液具有强氧化性,能够氧化碱式滴定管的橡胶管;根据反应的颜色变化判断滴定终点;
(5)根据反应方程式找出关系式,然后计算出三次滴定消耗的高锰酸钾溶液的平均体积,根据关系式计算出每片硫酸亚铁糖衣片中含有铁元素质量.
(2)酸性高锰酸钾具有强氧化性,将Fe2+氧化为Fe3+,被还原为Mn2+,同时生成水;
(3)用高锰酸钾溶液滴定,加入的酸不能具有氧化性,不能与高锰酸钾溶液反应;
(4)高锰酸钾溶液具有强氧化性,能够氧化碱式滴定管的橡胶管;根据反应的颜色变化判断滴定终点;
(5)根据反应方程式找出关系式,然后计算出三次滴定消耗的高锰酸钾溶液的平均体积,根据关系式计算出每片硫酸亚铁糖衣片中含有铁元素质量.
解答:解:(1)由于亚铁离子容易被氧气氧化,所以配制样品溶液时把水煮沸,除去溶解在水中的氧气,故答案为:除去溶解在水中的氧气;
(2)酸性高锰酸钾具有强氧化性,将Fe2+氧化为Fe3+,被还原为Mn2+,同时生成水,反应离子方程式为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
(3)由于利用高锰酸钾溶液进行滴定来测量亚铁离子的含量,加入的酸不能具有氧化性,所以不可以用硝酸;盐酸中的氯离子具有还原性,能够被高锰酸钾氧化,对测定结果产生影响,所以不可以用盐酸;故实验中所用的KMO4溶液要进行酸化,用于酸化的酸是:B硫酸,
故选B;
(4)由于高锰酸钾溶液具有氧化性,不能使用碱式滴定管,所以量取高锰酸钾溶液使用的是酸式滴定管;反应结束前溶液是无色的,反应结束时再滴入高锰酸钾溶液,溶液由无色变为浅紫色,所以滴定终点现象是:滴入最后一滴高锰酸钾溶液后,溶液由无色变为浅紫色,且半分钟内不褪色,
故答案为:酸式滴定管;滴入最后一滴高锰酸钾溶液后,溶液由无色变为浅紫色,且半分钟内不褪色;
(5)三次滴定消耗的高锰酸钾溶液都是有效的,平均体积为:
=21.43mL,消耗的高锰酸钾的物质的量是:0.02143L×0.0010mol/L=2.143×10-5mol,
根据反应:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,可得关系式:5Fe2+~MnO4-,n(Fe2+)=5n(MnO4-)=5×2.143×10-5mol,250mL溶液中含有的亚铁离子的物质的量是:5×2.143×10-5mol×
=5×2.143×10-4mol,
10片硫酸亚铁糖衣片中亚铁离子的质量是:m(Fe2+)=56×5×2.143×10-4g≈0.06g=60mg,每片每片硫酸亚铁糖衣片中含有铁元素的质量为:
=6mg,
故答案为:6.
(2)酸性高锰酸钾具有强氧化性,将Fe2+氧化为Fe3+,被还原为Mn2+,同时生成水,反应离子方程式为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
(3)由于利用高锰酸钾溶液进行滴定来测量亚铁离子的含量,加入的酸不能具有氧化性,所以不可以用硝酸;盐酸中的氯离子具有还原性,能够被高锰酸钾氧化,对测定结果产生影响,所以不可以用盐酸;故实验中所用的KMO4溶液要进行酸化,用于酸化的酸是:B硫酸,
故选B;
(4)由于高锰酸钾溶液具有氧化性,不能使用碱式滴定管,所以量取高锰酸钾溶液使用的是酸式滴定管;反应结束前溶液是无色的,反应结束时再滴入高锰酸钾溶液,溶液由无色变为浅紫色,所以滴定终点现象是:滴入最后一滴高锰酸钾溶液后,溶液由无色变为浅紫色,且半分钟内不褪色,
故答案为:酸式滴定管;滴入最后一滴高锰酸钾溶液后,溶液由无色变为浅紫色,且半分钟内不褪色;
(5)三次滴定消耗的高锰酸钾溶液都是有效的,平均体积为:
| 21.44mL+21.43mL+21.42mL |
| 3 |
根据反应:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,可得关系式:5Fe2+~MnO4-,n(Fe2+)=5n(MnO4-)=5×2.143×10-5mol,250mL溶液中含有的亚铁离子的物质的量是:5×2.143×10-5mol×
| 250 |
| 25 |
10片硫酸亚铁糖衣片中亚铁离子的质量是:m(Fe2+)=56×5×2.143×10-4g≈0.06g=60mg,每片每片硫酸亚铁糖衣片中含有铁元素的质量为:
| 60 |
| 10 |
故答案为:6.
点评:本题考查学生对实验原理与实验操作的理解、元素化合物性质、氧化还原反应滴定、化学计算等,难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力.

练习册系列答案
相关题目
铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水,但能溶于人体中的胃酸。
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
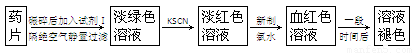
(1)试剂Ⅰ是____________。
(2)加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是________________________________________________________________________。
(3)在实验中发现放置一段时间,溶液的颜色会逐渐褪去。为了进一步探究溶液褪色的原因,甲、乙、丙三位同学首先进行了猜想:
|
编号 |
猜想 |
|
甲 |
溶液中的+3价Fe又被还原为+2价Fe |
|
乙 |
溶液中的SCN-被过量的氯水氧化 |
|
丙 |
新制的氯水具有漂白性,将该溶液漂白 |
基于乙同学的猜想,请设计实验方案,验证乙同学的猜想是否正确。写出有关的实验操作、预期现象和结论。(不一定填满,也可以补充)
|
编号 |
实验操作 |
预期现象和结论 |
|
① |
|
|
|
② |
|
|
|
③ |
|
|