题目内容
化学反应原理对于工业生产和科研有重要意义
I、下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
请回答:
(1)反应①是 (填“吸热”或“放热”)反应。
(2)据反应①与②可推导出K1、K2与K3之间的关系,则K3=__________(用K1、K2表示)。
(3)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有 _____(填写字母序号)。
A.缩小反应容器的容积
B.扩大反应容器的容积
C.升高温度
D.使用合适的催化剂
E.设法减小平衡体系中的CO的浓度
(4)若反应③的逆反应速率与时间的关系如图所示:
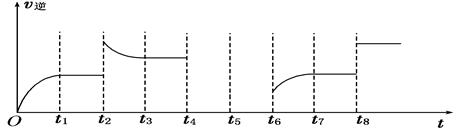
①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时__________________; t8时__________________。
②若t4时降压, t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线。
II、(5)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2.某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料.已知该装置的阳极反应为:4OH--4e-=O2↑+2H2O,则阴极反应为 。
(6)某空间站能量转化系统的局部如图所示,其中的燃料电池采用KOH溶液作电解液。
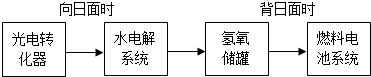
如果某段时间内,氢氧储罐中共收集到33.6L气体(已折算成标准状况),则该段时间内水电解系统中转移电子的物质的量为 mol。
I、下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
| 化学反应 | 平衡常数 | 温度 | |
| 973 K | 1173 K | ||
①Fe(s)+CO2(g) FeO(s)+CO(g) FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) FeO(s)+H2(g) FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
③CO(g) +H2O(g) CO2(g) +H2(g) CO2(g) +H2(g) | K3 | ? | ? |
请回答:
(1)反应①是 (填“吸热”或“放热”)反应。
(2)据反应①与②可推导出K1、K2与K3之间的关系,则K3=__________(用K1、K2表示)。
(3)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有 _____(填写字母序号)。
A.缩小反应容器的容积
B.扩大反应容器的容积
C.升高温度
D.使用合适的催化剂
E.设法减小平衡体系中的CO的浓度
(4)若反应③的逆反应速率与时间的关系如图所示:

①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时__________________; t8时__________________。
②若t4时降压, t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线。
II、(5)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2.某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料.已知该装置的阳极反应为:4OH--4e-=O2↑+2H2O,则阴极反应为 。
(6)某空间站能量转化系统的局部如图所示,其中的燃料电池采用KOH溶液作电解液。

如果某段时间内,氢氧储罐中共收集到33.6L气体(已折算成标准状况),则该段时间内水电解系统中转移电子的物质的量为 mol。
(1)吸热
(2)
(3)CE
(4)①升高温度或增大CO2的浓度(增大H2的浓度);使用催化剂或增大压强
②
(5)2CO2+4e-+2H2O═2CO+4OH-(或CO2+2e-+H2O═CO+2OH-)(6)2mol
(2)

(3)CE
(4)①升高温度或增大CO2的浓度(增大H2的浓度);使用催化剂或增大压强
②

(5)2CO2+4e-+2H2O═2CO+4OH-(或CO2+2e-+H2O═CO+2OH-)(6)2mol
试题分析:(1)在反应①中随着温度的升高平衡常数增大,这说明升高温度平衡向正反应方向移动,因此正方应是吸热反应。
(2)根据反应①②并依据盖斯定律可知②-①即得到反应③,所以平衡常数之间的关系为K3=
 。
。(3)根据表中数据可知,随着温度的升高K1逐渐增大,而K2逐渐减小,所以K3逐渐减小,这说明升高温度反应③向逆反应方向移动,因此正方应是放热反应。由于正方应是体积不变的可逆反应,所以要使平衡向逆反应方向移动,则可以升高温度或增大生成物的浓度或减小反应物的浓度,而压强和催化剂不能改变平衡,故答案选CE。
(4)①根据图像可知,t2时逆反应速率瞬间增大,然后逐渐减小,说明平衡向逆反应方向移动,由于正方应是体积不变的放热的可逆反应,所以改变的条件是升高温度或增大CO2的浓度(增大H2的浓度)。t8时逆反应速率瞬间增大,但平衡不移动,由于正方应是体积不变的放热的可逆反应,所以改变的条件是使用催化剂或增大压强。
②若t4时降压,反应速率均减小,但平衡不移动。t6时增大反应物的浓度,平衡向正反应方向移动,逆反应速率逐渐增大,因此t4~t6时逆反应速率与时间的关系线为
 。
。(5)电解池中阳极失去电子发生氧化反应,阴极得到电子发生还原反应,所以根据总反应式可知阴极是CO2得到电子被还原为CO,电极反应式为CO2+2e-+H2O═CO+2OH-。
(6)水电解生成氢气和氧气,所以氢氧储罐中共收集到33.6L气体应该是氢气与氧气的混合气,其中氧气是11.2L,氢气是22.4L,氢气的物质的量是1mol,转移2mol电子。

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目




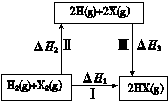

 H+(aq) +CH3COO-(aq) △H2="+1.3" kJ/mol
H+(aq) +CH3COO-(aq) △H2="+1.3" kJ/mol
