题目内容
【题目】镁的化合物在化工生产和药物合成上有重要用途。某兴趣小组以一种工业废渣(主要成分为MgCO3、MgSiO3和少量Fe的氧化物)为原料制备MgCO3·3H2O。实验过程如下:

(1)滤渣的成分为________(填化学式),过滤装置在使用一段时间后需用NaOH溶液清洗,用化学方程式表示其清洗原理:____________________________。
(2)加入H2O2的目的是________________________,一段时间后,溶液中有气泡出现并放热,则产生气泡的原因是_______________________________。
(3)萃取分液中要用到分液漏斗,分液漏斗在使用前须洗干净并________。
【答案】H2SiO3 H2SiO3+2NaOH===Na2SiO3+2H2O将Fe2+氧化成Fe3+Fe3+催化H2O2分解检漏
【解析】
废渣主要成分为MgCO3、MgSiO3和少量Fe的氧化物,加入40%的硫酸酸溶,过滤后滤液中含有硫酸镁、硫酸亚铁、过量的硫酸,滤渣为硅酸沉淀,滤液中加入H2O2氧化亚铁离子,然后加入有机萃取剂萃取Fe3+,分液后可除去溶液中的Fe3+,分液后水溶液中含有Mg2+,过滤后在滤液中加入碳酸钠溶液,可生成MgCO3沉淀,干燥后得到MgCO33H2O。以此解答该题。
(1)根据以上分析可知废渣的成分为硅酸,化学式为H2SiO3,硅酸和氢氧化钠反应生成硅酸钠和水,反应的化学方程式为H2SiO3+2NaOH=Na2SiO3+2H2O;
(2)在酸性条件下,H2O2氧化亚铁离子为铁离子,本身被还原为水,反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O,一段时间后,溶液中有气泡出现并放热是铁离子催化过氧化氢分解生成氧气;
(3)由于分液漏斗有活塞开关,故使用前需要检查是否漏液。

 阅读快车系列答案
阅读快车系列答案【题目】工业上以锂辉石为原料生产碳酸锂的部分工业流程如下:
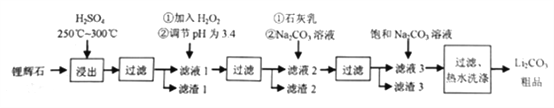
已知:①锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量FeO、MgO等。
②Li2O·Al2O3·4SiO2+H2SO4![]() Li2SO4+Al2O3·4SiO2·H2O
Li2SO4+Al2O3·4SiO2·H2O
③某些物质的溶解度(S)如下表所示。
T℃ | 20 | 40 | 60 | 80 |
S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
④Fe3+完全沉淀时pH为3.4
(1)为提高原料浸出速率,除升高温度外还可采取的措施是__________(任写一条)。
(2)在滤液1中加入H2O2的目的是__________(用离子方程式表示);调节pH最佳试剂是__________(填序号 )。
A.CuO B.CuCO3 C.MgO D.NH3·H2O
(3)从滤渣中分离出Al2O3的流程如下图所示,请写出生成沉淀的离子方程式__________。
![]()
(4)向滤液2中加入Na2CO3溶液的作用是__________。
(5)“过滤、热水洗涤”步骤中,“热水洗涤”的原因是__________;证明沉淀已洗净的操作是__________。





