题目内容
(2012?丹东模拟)已知电离平衡常数:H2CO3>HClO>HCO3-,氧化性:HClO>Cl2>Br2>Fe3+>I2.下列有关离子反应或离子方程式的叙述中,正确的是( )
分析:A.能使PH试纸显深红色的溶液呈酸性;
B.向溴水中加入足量氯化亚铁溶液,生成Fe3+;
C.酸性H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳生成HCO3-;
D.根据氧化性判断参加反应的离子.
B.向溴水中加入足量氯化亚铁溶液,生成Fe3+;
C.酸性H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳生成HCO3-;
D.根据氧化性判断参加反应的离子.
解答:解:A.能使PH试纸显深红色的溶液呈酸性,在酸性条件下离子之间不发生任何反应,可大量共存,故A正确;
B.向溴水中加入足量氯化亚铁溶液,生成Fe3+,溶液呈黄色,故B错误;
C.酸性H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳生成HCO3-,故C错误;
D.氧化性:HClO>Cl2>Br2>Fe3+>I2,向FeI2溶液中滴加少量氯水,反应的离子方程式为:2I-+Cl2=I2+2Cl-,故D错误.
故选A.
B.向溴水中加入足量氯化亚铁溶液,生成Fe3+,溶液呈黄色,故B错误;
C.酸性H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳生成HCO3-,故C错误;
D.氧化性:HClO>Cl2>Br2>Fe3+>I2,向FeI2溶液中滴加少量氯水,反应的离子方程式为:2I-+Cl2=I2+2Cl-,故D错误.
故选A.
点评:本题考查离子共存问题,题目难度中等,本题注意把握题给信息,为解答该题的关键,也是易错点,学习中注意把握常见离子的性质.

练习册系列答案
相关题目

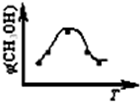 (2012?丹东模拟)能源短缺是人类面临的重大问题.甲醇是一种可再生能源.具有广泛的开发和应用前景.因此甲醇被称为21世纪的新型燃料.
(2012?丹东模拟)能源短缺是人类面临的重大问题.甲醇是一种可再生能源.具有广泛的开发和应用前景.因此甲醇被称为21世纪的新型燃料. (2012?丹东模拟)某种兴奋剂的结构如图所示,下列说法正确的是( )
(2012?丹东模拟)某种兴奋剂的结构如图所示,下列说法正确的是( )