题目内容
(2012?丹东模拟)下列说法正确的是( )
分析:A、铵根离子水解程度小结合的离子对铵根离子的水解的影响分析判断;
B、水电离出的c(H+)=1×10-amol/L,若a>7时水的电离被抑制,酸或碱都能抑制水的电离;
C、依据溶液中的电荷守恒分析判断;
D、程度溶解平衡温度不变,溶度积不变,加入氯化钠平衡左移,离子浓度乘积不变;
B、水电离出的c(H+)=1×10-amol/L,若a>7时水的电离被抑制,酸或碱都能抑制水的电离;
C、依据溶液中的电荷守恒分析判断;
D、程度溶解平衡温度不变,溶度积不变,加入氯化钠平衡左移,离子浓度乘积不变;
解答:解:A、相同物质的量浓度的下列溶液中,①NH4Al(SO4)2溶液中铝离子水解显酸性抑制铵根离子的水解,②NH4Cl溶液中氯离子不影响铵根离子水解、③CH3COONH4溶液中醋酸根水解显碱性,促进铵根离子的水解、④NH3?H2O溶液中存在电离平衡电离程度较小,所以铵根离子浓度大小顺序是:①>②>③>④,故A正确;
B、某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,说明水的电离被抑制,酸或碱都能抑制水的电离,所以PH可以是a,也可以是14-a,故B错误;
C、物质的量浓度相等的 H2S 和 NaHS 混合溶液中存在电荷守恒为:c (Na+)+c(H+)=2c (S2-)+c (HS-)+c (OH-),故C错误;
D、AgCl悬浊液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),往其中加入少量 NaCl粉末,平衡会向左移动,但温度不同溶度积不同,所以氯离子浓度增大,银离子浓度减少,溶液中离子的总浓度不变,故D错误;
故选A.
B、某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,说明水的电离被抑制,酸或碱都能抑制水的电离,所以PH可以是a,也可以是14-a,故B错误;
C、物质的量浓度相等的 H2S 和 NaHS 混合溶液中存在电荷守恒为:c (Na+)+c(H+)=2c (S2-)+c (HS-)+c (OH-),故C错误;
D、AgCl悬浊液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),往其中加入少量 NaCl粉末,平衡会向左移动,但温度不同溶度积不同,所以氯离子浓度增大,银离子浓度减少,溶液中离子的总浓度不变,故D错误;
故选A.
点评:不同考查了盐类水解的离子浓度大小比较,水的电离平衡影响因素,溶液中电荷守恒的应用,沉淀溶解平衡的溶度积常数的应用.

练习册系列答案
相关题目

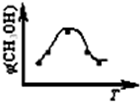 (2012?丹东模拟)能源短缺是人类面临的重大问题.甲醇是一种可再生能源.具有广泛的开发和应用前景.因此甲醇被称为21世纪的新型燃料.
(2012?丹东模拟)能源短缺是人类面临的重大问题.甲醇是一种可再生能源.具有广泛的开发和应用前景.因此甲醇被称为21世纪的新型燃料. (2012?丹东模拟)某种兴奋剂的结构如图所示,下列说法正确的是( )
(2012?丹东模拟)某种兴奋剂的结构如图所示,下列说法正确的是( )