题目内容
【题目】在一定条件下,将3 mol A 和 1 mol B 两种气体混合于固定容积为 2 L 的密闭容器中,发生如下反应: 3A(g)+B(g) ![]() xC(g)+2D(g)。 2 min 末该反应达到平衡,测得生成 0.8 mol D,0.4 molC。下列判断正确的是( )
xC(g)+2D(g)。 2 min 末该反应达到平衡,测得生成 0.8 mol D,0.4 molC。下列判断正确的是( )
A. x=2 B. 2 min 时, A 的浓度为 1.2mol·L-1
C. 2 min 内 A 的反应速率为 0.6 mol·L-1·min-1 D. B 的转化率为 60%
【答案】B
【解析】由3A(g)+B(g) ![]() xC(g)+2D(g)知2 min末该反应达到平衡,测得生成0.8 molD和0.4 molC,可以知道
xC(g)+2D(g)知2 min末该反应达到平衡,测得生成0.8 molD和0.4 molC,可以知道![]() ,计算得出
,计算得出![]() ,则
,则
3A(g)+B(g)![]() 4C(g)+2D(g)
4C(g)+2D(g)
开始 3 1 0 0
转化 0.6 0.2 0.8 0.4
平衡 2.4 0.8 0.8 0.4
A.由上述分析可以知道, x=4,故A错误;B. 2 min时,A的浓度为![]() ,故B错误;C. 2 min内A的反应速率为
,故B错误;C. 2 min内A的反应速率为 ,故C错误;D.B的转化率为
,故C错误;D.B的转化率为![]() ,所以D错;所以D选项是正确的。
,所以D错;所以D选项是正确的。

【题目】某同学设计计如图所示装罝(部分夹持装置己略去)进行实验探究: 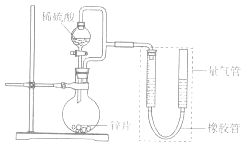
(1)用上述装置探究影响化学反应速率的因素.以生成9.0mL气体为计时终点,结果为t1>t2 .
序号 | V(H2SO4)/mL | C(H2SO4)/molL﹣1 | t/s |
I | 40 | 1 | t1 |
II | 40 | 4 | t2 |
①比较实验I和Ⅱ可以得出的实验结论是 .
②若将锌片换成含杂质的粗锌片,其他条件使其与上述一致,所测得的反应速率均大于上述实验对应的数据.粗锌片中所含杂质可能是(填序号).
A.二氧化硅 B.银 C.铜 D.石墨
(2)用上述装置验证生铁在潮湿空气中会发生吸氧腐蚀 ①圆底烧瓶中的试剂可选用(填序号)
A.稀HCl B.NaCl溶液 C.乙醇 D.NaOH溶液
②能证明生铁在潮湿空气中会发生吸氧腐蚀的现象是 .
