题目内容
在一定温度下,有盐酸、硫酸、醋酸三种溶液,请按要求回答下列问题:
(1)当三种酸的物质的量浓度相同时,电离出来的c(H+)最大的是__________。
(2)若三者电离出来的c(H+)相同时,三种酸的物质的量浓度最小的是________。
(3)pH相同、体积相同的醋酸溶液和盐酸分别与足量的锌反应,刚开始反应时的反应速率的大小关系为______(填“相等”或者“不等”),相同状况下产生氢气的体积最大的酸是______。pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH仍相同,则m和n的关系是:m n(填“>”、“=”、“<”)
(4)同体积、同物质的量浓度的醋酸和盐酸两种酸,分别中和同浓度的NaOH溶液,消耗NaOH的体积大小关系为 (填“相等”或者“不等”)
(1)当三种酸的物质的量浓度相同时,电离出来的c(H+)最大的是__________。
(2)若三者电离出来的c(H+)相同时,三种酸的物质的量浓度最小的是________。
(3)pH相同、体积相同的醋酸溶液和盐酸分别与足量的锌反应,刚开始反应时的反应速率的大小关系为______(填“相等”或者“不等”),相同状况下产生氢气的体积最大的酸是______。pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH仍相同,则m和n的关系是:m n(填“>”、“=”、“<”)
(4)同体积、同物质的量浓度的醋酸和盐酸两种酸,分别中和同浓度的NaOH溶液,消耗NaOH的体积大小关系为 (填“相等”或者“不等”)
(1)H2SO4(硫酸) (2) H2SO4(硫酸) (3)相等、CH3COOH(醋酸)、> (4)相等
试题分析:(1)当三种酸的物质的量浓度相同时,由于盐酸和硫酸是强酸,完全电离,硫酸又是二元酸,而醋酸是弱酸,不完全电离,所以c(H+)最大的是硫酸。(2)三者电离出来的c(H+)相同时,因为醋酸为弱酸,其物质的量浓度远大于溶液中c(H+),而盐酸是一元强酸,硫酸是二元强酸,所以三者的物质的量浓度大小顺序为:c(CH3COOH)>c(HCl)>c(H2SO4),硫酸物质的量浓度最小。(3)pH相同则氢离子浓度相等,所以刚开始反应时的反应速率相等;因为醋酸是弱酸,加水稀释促进电离,稀释相同倍数时H+浓度比盐酸中H+浓度大,只有稀释倍数越大,才能使其和盐酸稀释后的H+浓度相同即pH仍相等,故m>n。(4)醋酸和盐酸的体积、物质的量均相等时,其溶质的物质的量也相等,能中和的NaOH的物质的量也相等,而NaOH溶液的浓度相同,故消耗的NaOH溶液的体积相等。

练习册系列答案
相关题目
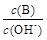 ②
②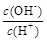 ③c(H+)和c(OH-)的乘积 ④OH-的物质的量
③c(H+)和c(OH-)的乘积 ④OH-的物质的量