题目内容
14.下列关于硅单质及其化合物的说法正确的是( )①硅是构成一些岩石和矿物的基本元素,在自然界中只以化合态的形式存在
②陶瓷、水泥、玻璃、水晶饰物都是硅酸盐制品
③硅的最高价氧化物不与任何酸反应
④SiO2高熔点、硬度大,是原子晶体,用作光导纤维
⑤硅的气态氢化物没有甲烷稳定.
| A. | ①②⑤ | B. | ②③④ | C. | ①④⑤ | D. | ③④⑤ |
分析 ①自然界中无游离态的硅;
②水晶主要成分是二氧化硅;
③二氧化硅常温下能够与氢氟酸反应;
④二氧化硅为氧原子与硅原子通过共价键形成原子晶体,结合原子晶体性质解答;
⑤非金属性越强,气体氢化物越稳定.
解答 解:①岩石和矿物中含有硅酸盐、二氧化硅,所以岩石和矿物的基本元素有硅元素,硅自然界中只以化合态的形式存,故正确;
②水晶主要成分是二氧化硅,二氧化硅为氧化物,故错误;
③二氧化硅常温下能够与氢氟酸反应生成四氟化硅和水,故错误;
④二氧化硅为氧原子与硅原子通过共价键形成原子晶体,原子晶体高熔点、硬度大,二氧化硅是制作光导纤维主要原料,故正确;
⑤碳的非金属性强于硅,所以甲烷稳定性强于硅烷,故正确;
故选:C.
点评 本题考查了硅气体化合物性质,侧重考查学生对基础知识掌握熟练程度,掌握基础是解题关键,题目难度不大.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
4.下列说法不正确的是( )
| A. | 硫酸的摩尔质量与6.02×1023个磷酸分子的质量在数值上相等 | |
| B. | 6.02×1023个N2和6.02×1023个O2的质量比等于7:8 | |
| C. | 常温、常压下,0.5×6.02×1023个二氧化碳分子质量是44 g | |
| D. | 3.2 g O2所含的原子数目约为0.2×6.02×1023 |
5.化学是人类创造新物质的工具.下列各种物质的现代工业生产原理或过程的描述正确的是( )
| A. | 工业上以硫或二硫化亚铁(FeS2)为原料制备硫酸 | |
| B. | 电解NaCl溶液制备金属钠同时得到Cl2 | |
| C. | 用H2或CO还原Al2O3制备金属铝 | |
| D. | 用裂化的方法生产大量乙烯 |
2.下列关于生活中化学的认识合理的是( )
| A. | 福尔马林是一种良好的杀毒剂,也可用来消毒自来水 | |
| B. | 现在家用的清洁燃料主要有两类:一类是压缩天然气,另一类为液化石油气,他们都属于有机物 | |
| C. | 为了提高加酶洗衣粉的洗涤效果,先用热的自来水溶解洗衣粉 | |
| D. | 随着人们生活节奏的加快,方便的小包装食品已被广泛接受.为了防止中秋月饼等富脂食品氧化变质,延长食品的保质期,正确的做法是在包装袋中常放入生石灰 |
9.为了探究FeS04和Cu(N03)2的混合物中各组分的含量,现设计如下流程.
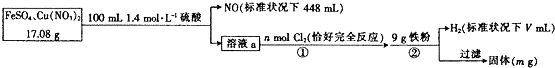
下列叙述中错误的是( )

下列叙述中错误的是( )
| A. | n=0.02 | |
| B. | y=2240 | |
| C. | 原混合物中FeS04的质量分数约为89% | |
| D. | m=3.2 |
19.有一在空气中暴露过的KOH固体,含水2.8%,K2CO37.2%.取1g该样品投入25mL 2mol/L HCl中,中和多余的HCl又用去1.07mol/L的KOH溶液30.8ml,蒸发中和后的溶液,所得固体的质量是( )
| A. | 4.50g | B. | 4.00g | C. | 3.73g | D. | 7.45g |
3.某原电池由M、N两根电极导线和电解质溶液组成,工作时,M电极变粗,N电极变细,由此判断该电池中电极材料和电解质溶液可能是( )
| M电极 | N电极 | 电解质溶液 | |
| A | 锌 | 铜 | 稀硫酸 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 锌 | 铁 | 硝酸铁溶液 |
| A. | A | B. | B | C. | C | D. | D |
16.若35.4g 铜银合金与2L 0.5mol/L 的硝酸溶液恰好完全反应,则收集的NO在标准状况下的体积是( )
| A. | 11.2 L | B. | 6.27 L | C. | 5.6 L | D. | 无法确定 |