题目内容
【题目】已知:从石油中获得A是目前工业上生产A的主要途径,A的产量通常用来衡量一个国家的石油化工发展水平。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
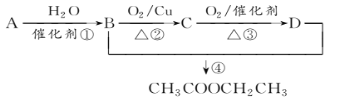
回答下列问题:
(1)写出A的结构简式______________。
(2)B、D分子中的官能团名称分别是_______________、________________。
(3)写出下列反应的反应类型:①_________,②________,④__________。
(4)写出下列反应的化学方程式:
①________________________________________________________________;
②________________________________________________________________。
③________________________________________________________________。
【答案】CH2=CH2 羟基 羧基 加成反应 氧化反应 酯化反应(或取代反应) CH2=CH2+H2O![]() CH3CH2OH 2CH3CH2OH+O2
CH3CH2OH 2CH3CH2OH+O2![]() 2CH3CHO+2H2O CH3CH2OH + CH3COOH
2CH3CHO+2H2O CH3CH2OH + CH3COOH![]() CH3COOCH2CH3+ H2O
CH3COOCH2CH3+ H2O
【解析】
由信息可知A为CH2=CH2,结合合成路线图可知,A与水发生加成反应生成B为CH3CH2OH,B发生氧化反应生成C为CH3CHO,C发生氧化反应生成D为CH3COOH,B与D发生酯化反应生成CH3COOCH2CH3,以此解答该题。
(1)由以上分析可知A为CH2═CH2;
答案为:CH2═CH2。
(2)B为CH3CH2OH,B中官能团为羟基,D为CH3COOH,D中官能团为羧基;
答案为羟基、羧基。
(3)反应①的反应类型为加成反应、,②的反应类型为氧化反应,④的反应类型为酯化反应(或取代反应);
答案为加成反应,氧化反应,酯化反应(或取代反应);
(4)①乙烯与水发生加成反应生成乙醇,方程式为CH2═CH2+H2O![]() CH3CH2OH;
CH3CH2OH;
答案为CH2═CH2+H2O![]() CH3CH2OH。
CH3CH2OH。
②乙醇发生催化氧化生成乙醛,方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
答案为2CH3CH2OH+O2![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。
③乙酸与乙醇发生酯化反应,方程式为CH3CH2OH + CH3COOH![]() CH3COOCH2CH3+ H2O;
CH3COOCH2CH3+ H2O;
答案为CH3CH2OH + CH3COOH![]() CH3COOCH2CH3+ H2O。
CH3COOCH2CH3+ H2O。

 阅读快车系列答案
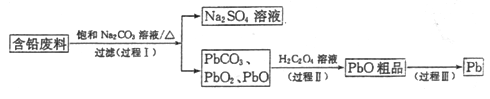
阅读快车系列答案【题目】硫铁矿烧渣的主要成分为Fe2O3、Fe3O4,以及少量SiO2、Al2O3等。由硫铁矿烧渣制备铁红(Fe2O3)的一种工艺流程如下:

已知:还原焙烧时,大部分Fe2O3、Fe3O4转化为FeO。
几种离子开始沉淀和完全沉淀时的pH如下表所示:
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe2+ | 7.6 | 9.7 |
Fe3+ | 2.7 | 3.7 |
Al3+ | 3.8 | 4.7 |
(1)“酸浸、过滤”步骤中所得滤液中的金属阳离子有(填离子符号)________________。
(2)Fe粉除调pH外,另一个作用是___________;Fe粉调节溶液的pH为__________。
(3)“沉淀、过滤”步骤中生成FeCO3的离子方程式为_______________________________;
所得滤液的主要溶质是(填化学式)_______________。
(4)高温条件下,“氧化”步骤中发生反应的化学方程式为______________________________。
【题目】下表是元素周期表的一部分,请回答有关问题:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
2 | ① | ② | ③ | ④ | |||
3 | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)第2周期的8种元素中,第一电离能介于①元素和③元素间的元素有__种。
(2)表中能形成两性氢氧化物的元素是___(填元素名称![]() ,写出该元素的单质与⑨最高价氧化物的水化物反应的离子方程式___。
,写出该元素的单质与⑨最高价氧化物的水化物反应的离子方程式___。
(3)②、⑤、⑦、⑨六种元素的最高价氧化物的水化物中,按碱性减弱酸性增强的顺序排列为(用化学式表示)___。
(4)④元素与⑩元素两者质子数之差是___。
(5)请写出③的气体氢化物发生催化氧化的化学方程式___。
(6)请写出⑥元素的最高价氧化物的水化物与⑧元素的最高价氧化物的水化物反应的离子方程式___。