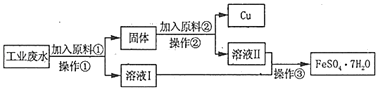
题目内容
【题目】2008年,三鹿等多家乳制品企业为使蛋白质含量检测合格而加入三聚氰胺,使多名儿童患肾结石,实验室可用下列实验装置测定三聚氰胺的分子式。
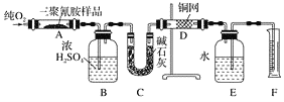
已知三聚氰胺的相对分子质量为126。取1.26 g三聚氰胺样品,放在纯氧中充分燃烧,生成二氧化碳、水、氮气,实验测得装置B增重0.54g,C增重1.32g,排入F中水的体积为672 mL(可按标准状况计算)。
(1)E装置的作用是_____。
(2)需要加热的装置是____(填字母代号)。
(3)装置D的作用是_____。
(4)F处读数时应该注意的是____、_____。
(5)三聚氰胺的分子式为____。
【答案】用来排水,以测定氮气的体积 AD 吸收未反应的氧气 量筒内的液面与广口瓶内的液面相平 视线与凹液面最低处相切 C3N6H6
【解析】
三聚氰胺在氧气中燃烧,生成的水被B中的浓硫酸吸收,生成的二氧化碳被C中的碱石灰吸收,过量的氧气被D中的铜网吸收,生成的N2进入E中,把E中的水排入F中。通过测定生成的水、二氧化碳和氮气的量,就可以确定三聚氰胺的最简式,再根据三聚氰胺的相对分子质量,就可以确定其分子式。
(1)E装置的作用是用来排水,以测定氮气的体积。
(2)三聚氰胺燃烧,需要加热硬质玻璃管A,吸收氧气要通过灼热的铜网,所以D也需要加热,所以需要加热的装置是AD。
(3)装置D的作用是吸收未反应的氧气,以防干扰氮气体积的测定。
(4)F处读数时,应该使量筒内的液面与广口瓶内的液面相平以保证压强一定,同时还要注意视线与凹液面最低处相切。
(5)装置B增重0.54g,即生成水0.54g,即0.03molH2O;C增重1.32g,即生成CO20.03mol;排入F中水的体积即为生成的氮气的体积,为672 mL,即0.03mol,所以三聚氰胺中C、H、N的原子个数比为0.03:0.06:0.06=1:2:2,所以三聚氰胺的最简式为CH2N2,三聚氰胺的相对分子质量为126,所以三聚氰胺的分子式为C3N6H6。