题目内容
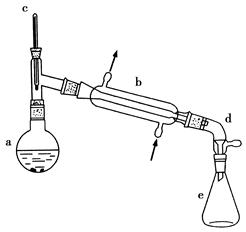
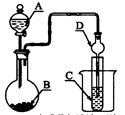
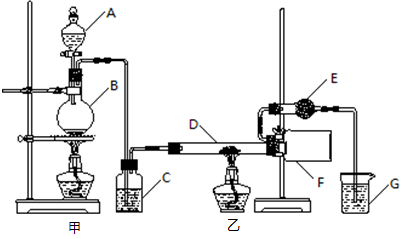
氢化钙(CaH2)固体是登山运动员常用的能源提供剂。氢化钙要密封保存,一旦接触到水就发生反应生成氢氧化钙和氢气。氢化钙通常用氢气与金属钙加热制取,图1是模拟制取装置:
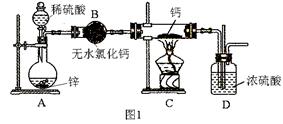
(1)装置B的作用是 ;装置D的作用是 ;
(2)利用图1实验装置进行实验,实验步骤如下:检查装置气密性后装入药品;打开分液漏斗活塞, (请按正确的顺序填入下列步骤的序号)。
①加热反应一段时间 ②收集气体并检验其纯度
③关闭分液漏斗活塞 ④停止加热,充分冷却
(3)为了确认进入装置C的氢气已经干燥,应在B、C之间再接一装置,该装置中加入的试剂是: 。
(4)甲同学设计一个实验,测定上述实验中得到的氢化钙的纯度(杂质中不含钙元素。请完善下列实验步骤:
①样品称量;②加入________溶液(填化学式),搅拌、过滤;③________(填操作名称);④_______ (填操作名称); ⑤称量碳酸钙。
(5)乙同学利用注射器测量氢化钙和水反应氢气体积的方法,测定上述实验中得到的氢化钙的纯度。他称取46 mg 所制得的氢化钙样品,记录开始时注射器活栓停留在10.00mL刻度处,反应结束后充分冷却,活栓最终停留在57.04mL刻度处(上述气体体积均在标准状况下测定)。试通过计算求样品中氢化钙的纯度: 。
(6)请你再设计一种氢化钙纯度的测定方法: 。

(1)装置B的作用是 ;装置D的作用是 ;
(2)利用图1实验装置进行实验,实验步骤如下:检查装置气密性后装入药品;打开分液漏斗活塞, (请按正确的顺序填入下列步骤的序号)。
①加热反应一段时间 ②收集气体并检验其纯度
③关闭分液漏斗活塞 ④停止加热,充分冷却
(3)为了确认进入装置C的氢气已经干燥,应在B、C之间再接一装置,该装置中加入的试剂是: 。
(4)甲同学设计一个实验,测定上述实验中得到的氢化钙的纯度(杂质中不含钙元素。请完善下列实验步骤:
①样品称量;②加入________溶液(填化学式),搅拌、过滤;③________(填操作名称);④_______ (填操作名称); ⑤称量碳酸钙。
(5)乙同学利用注射器测量氢化钙和水反应氢气体积的方法,测定上述实验中得到的氢化钙的纯度。他称取46 mg 所制得的氢化钙样品,记录开始时注射器活栓停留在10.00mL刻度处,反应结束后充分冷却,活栓最终停留在57.04mL刻度处(上述气体体积均在标准状况下测定)。试通过计算求样品中氢化钙的纯度: 。
(6)请你再设计一种氢化钙纯度的测定方法: 。
(1)除去氢气中的水蒸气;防止空气中的水蒸气进入C装置(2)②①④③(3)无水硫酸铜 (或其他合理答案)(4)Na2CO3(K2CO3或其他合理答案)洗涤 烘干(干燥)(5)91.3% (2分)(6)称取一定量的样品(m1 g),加入盐酸溶液至不再冒气泡,然后将溶液蒸发得到氯化钙固体(m2 g),根据m1、m2即可得到氢化钙的纯度。(或其他合理答案)
试题分析:氢化钙要密封保存,一旦接触到水就发生反应生成氢氧化钙和氢气,H2在发生加热反应之前需要干燥,一般用无水氯化钙,故装置B的作用是:除去氢气中的水蒸气,装置D的作用是:防止空气中的水蒸气进入C装置,故答案为:除去氢气中的水蒸气;防止空气中的水蒸气进入C装置(2)有气体参加加热或燃烧的反应需要首先验纯,实验完毕后先熄火、冷却,再停止气体生成,防止倒吸发生爆炸,故正确的操作顺序为:②①④③。(3)检验是否干燥用无水硫酸铜,因为无水硫酸铜遇水变蓝色现象很明显,故答案为:无水硫酸铜。(4)从最终称量碳酸钙可知,应加入碳酸钠溶液,使CaH2反应的同时得到碳酸钙沉淀,然后经过滤、洗涤、烘干、称量,确定纯度,故答案为:Na2CO3;洗涤、烘干。(5)由注射器D开始时活塞停留在10mL刻度处,反应结束后充分冷却,活塞最终停留57.04mL刻度处,可知生成氢气:57.04mL-10mL=47.04mL,所以氢气的质量
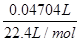 =2g/mol=0.0042g=4.2mg,设混合物中氢化钙的质量为x,生成氢气质量为y,则钙的质量为46mg-x,钙与水反应生成氢气质量为4.2mg-y,则:
=2g/mol=0.0042g=4.2mg,设混合物中氢化钙的质量为x,生成氢气质量为y,则钙的质量为46mg-x,钙与水反应生成氢气质量为4.2mg-y,则:CaH2+2H2O═Ca(OH)2+2H2↑
42 4
X Y
所以42:4=x:y,整理的y=
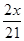
Ca+2H2O═Ca(OH)2+H2↑
40 2
46mg-x 4.2mg-y
所以40:2=(46mg-x):(4.2mg-y),将y=
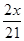 代入,解得x=42mg,所以样品中氢化钙的纯度为:
代入,解得x=42mg,所以样品中氢化钙的纯度为: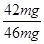 ×100%=91.30%,故答案为:91.3%
×100%=91.30%,故答案为:91.3%(6)称取一定量的样品(m1g),加入盐酸溶液至不再冒气泡(反应完全),然后将溶液蒸发得到氯化钙固体(m2g),根据m1、m2即可得到氢化钙的纯度,故答案为:称取一定量的样品(m1g),加入盐酸溶液至不再冒气泡(反应完全),然后将溶液蒸发得到氯化钙固体(m2g),根据m1、m2即可得到氢化钙的纯度。

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目