题目内容
【题目】短周期元素R、T、X、Y、Z在元素周期表的相对位置如下表所示,它们的最外层电子数之和为31。则下列判断正确的是

A.R位于元素周期表中第二周期第ⅣA族
B.原子半径:X<R<T
C.最简单气态氢化物稳定性:T>R>Y
D.最高价氧化物对应的水化物酸性:T>R>Y
【答案】C
【解析】
试题五种元素属于短周期元素,设R的最外层电子数为a,则T的最外层电子数a+1,X的为a-1,Y的为a,Z的为a+1,最外层电子数之和为31,即a+a+1+a-1+a+a+1=31,解得a=6,推出R:O,T:F,X:P,Y:S,Z:Cl,A、R位于第二周期ⅥA族元素,故错误;B、原子半径大小比较规律:看电子层数:电子层数越大,半径越大,电子层数相同,看原子序数:原子序数越大,半径越小,原子半径大小顺序:P>O>F,故错误;C、氢化物的稳定性,与非金属性强弱有关,非金属性越强,其氢化物越稳定,非金属性强弱:F>O>S,氢化物的稳定性:HF>H2O>H2S,故正确;D、非金属性越强,其最高价氧化物对应的水化物酸性越强,F非金属性强,没有正价,O在中学阶段没有正价,故错误。

 阅读快车系列答案
阅读快车系列答案【题目】乙酸正丁酯是一种优良的有机溶剂,广泛用于硝化纤维清漆中,在人造革、织物及塑料加工过程中用作溶剂,也用于香料工业。某化学兴趣小组在实验室用乙酸和正丁醇制备乙酸正丁酯,有关物质的相关数据及实验装置如下所示:
化合物 | 相对分子质量 | 密度(g/cm3) | 沸点(℃) | 溶解度(g/100 g水) |
冰醋酸 | 60 | 1.045 | 117.9 | 互溶 |
正丁醇 | 74 | 0.80 | 118.0 | 9 |
乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
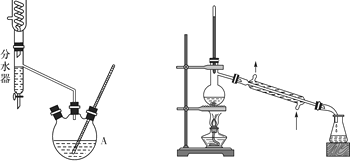
I II
分水器的操作方法:先将分水器装满水(水位与支管口相平),再打开活塞,准确放出一定体积的水。在制备过程中,随着加热回流,蒸发后冷凝下来的有机液体和水在分水器中滞留分层,水并到下层(反应前加入的)水中;有机层从上面溢出,流回反应容器。当水层增至支管口时,停止反应。
乙酸正丁酯合成和提纯步骤为:
第—步:取18.5 mL正丁醇和15.4 mL冰醋酸混合加热发生酯化反应,反应装置如图Ⅰ所示(加热仪器已省略);
第二步:依次用水、饱和Na2CO3溶液、水对烧瓶中的产品洗涤并干燥;
第三步:用装置Ⅱ蒸馏提纯。
请回答有关问题:
(1)第一步装置中除了加正丁醇和冰醋酸外,还需加入___________、______________。
(2)实验中使用分水器的优点有________________、 ___________。根据题中给出的相关数据计算,理论上,应该从分水器中放出来的水的体积约为___________。
(3)第二步用饱和Na2CO3溶液洗涤的目的是____________________________。
(4)第三步蒸馏产品时,应收集温度在_______________左右的馏分。若实验中得到乙酸正丁酯12.76 g,则乙酸正丁酯的产率为___________________。