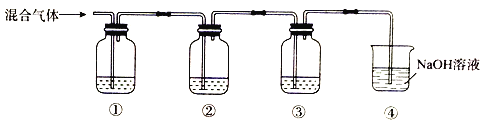
题目内容
【题目】高锰酸钾常用作消毒杀菌、水质净化剂等。某小组用软锰矿(主要含MnO2,还含有少量SiO2、Al2O3、Fe2O3等杂质)模拟工业制高锰酸钾流程如下。试回答下列问题。
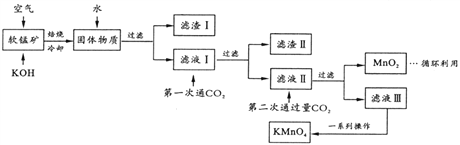
(1)配平焙烧时化学反应: □MnO2+□_____+□O2![]() □K2MnO4+□H2O;工业生产中采用对空气加压的方法提高MnO2利用率,试用碰撞理论解释其原因__________。
□K2MnO4+□H2O;工业生产中采用对空气加压的方法提高MnO2利用率,试用碰撞理论解释其原因__________。
(2)滤渣II 的成分有_______(化学式);第一次通CO2不能用稀盐酸代替的原因是_________。
(3)第二次通入过量CO2生成MnO2的离子方程式为_________。
(4)将滤液Ⅲ进行一系列操作得KMnO4。
由下图可知,从滤液Ⅲ得到KMnO4需经过_____、______、洗涤等操作。

(5)工业上按上述流程连续生产。含MnO2a%的软锰矿1吨,理论上最多可制KMnO4___吨。
(6)利用电解法可得到更纯的KMnO4。用惰性电极电解滤液II。
①电解槽阳极反应式为____________;
②阳极还可能有气体产生,该气体是__________。
【答案】 2 4 KOH 1 2 2 加压增大了氧气浓度,使单位体积内的活化分子数增加,有效碰撞次数增多,反应速率加快,使MnO2反应更充分 Al(OH)3、H2SiO3 稀盐酸可溶解Al(OH)3,不易控制稀盐酸的用量 3MnO42-+4CO2+2H2O=MnO2↓+2MnO4-+4HCO3- 蒸发结晶 趁热过滤 0.018a MnO42--e-=MnO4- O2
【解析】(1)MnO2中Mn的化合价为+4价,K2MnO4中Mn的化合价为+6价,O2中O的化合价为0价,生成物中都变成了-2价,根据得失电子守恒(化合价升降总数相等)得:MnO2前面系数为2,O2前面系数为1,K2MnO4前面系数为2;结合流程中焙烧时有KOH参与,所以未知的反应物应为KOH,根据原子守恒,KOH前面系数为4,水前面系数为2,故答案为:2 4 KOH 1 2 2。根据有效碰撞理论,加压可增大氧气浓度,使单位体积内的活化分子数增加,有效碰撞次数增多,反应速率加快,使MnO2反应更充分,所以工业生产中采用对空气加压的方法提高MnO2利用率。
(2)根据流程滤液I主要是K2MnO4溶液,还含有SiO32-和AlO2-等杂质离子,通入CO2发生反应:CO2+H2O+SiO32-=H2SiO3↓+CO32-、CO2+H2O+AlO2-=Al(OH)3↓+CO32-,所以滤渣II的成分有Al(OH)3和H2SiO3;因为第一次通入CO2目之一是生成Al(OH)3,而稀盐酸可溶解Al(OH)3,不易控制稀盐酸的用量,所以第一次通CO2不能用稀盐酸代替。
(3)第二次通入过量CO2生成MnO2,则MnO42-发生自身氧化还原反应,生成MnO2和MnO4-,因为CO2过量,所以还会生成HCO3-,故离子方程式为:3MnO42-+4CO2+2H2O=MnO2↓+2MnO4-+4HCO3-。
(4)滤液Ⅲ溶质主要是KMnO4与KHCO3,由图可看出,KMnO4溶解度受温度影响变化不大,而KHCO3溶解度,受温度影响变化较大,所以从滤液Ⅲ得到KMnO4需经过蒸发结晶、趁热过滤、洗涤、干燥等操作。
(5)根据Mn元素守恒,含MnO2a%的软锰矿1吨,理论上最多可制KMnO4:1×a%×![]() ≈0.018a(吨)。
≈0.018a(吨)。
(6)①滤液II主要为K2MnO4溶液,用惰性电极电解得到KMnO4,MnO42-在阳极上失电子发生氧化反应,生成MnO4-,故阳极电极反应式为:MnO42--e-=MnO4-;②溶液中的OH-也可能失电子发生氧化反应,生成氧气,故阳极还可能有O2产生。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案【题目】
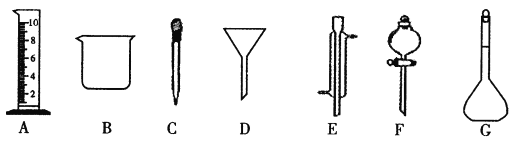
(1)写出仪器名称:E_____________,F_____________。
(2)下列实验操作中用到仪器D的是_________(选填下列选项的编号字母 )。
A.分离水和CC14的混合物 B.分离水和酒精的混合物 C.分离水和泥砂的混合物
Ⅱ.某课外兴趣小组需要200mL1mol/L的Na2CO3溶液,请回答下列问题:
(1)配制溶液所需仪器及药品:
应称取Na2CO3的质量 | 应选用容量瓶的规格 | 除容量瓶外还需要的其它玻璃仪器是上图中的______、_____及玻璃棒 |
(2)配制时,其正确的操作顺序是(用字母表示,每个操作只能用一次)______________。
A.将已冷却的溶液沿玻璃棒注入容量瓶中
B.用托盘天平准确称量所需Na2CO3的质量,倒入烧杯中,再加入适量水,用玻璃棒慢慢搅动,使其溶解(必要时可加热)
C.用适量水洗涤烧杯2-3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将容量瓶盖紧,振荡,摇匀
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(3)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?
没有进行C操作________;配制溶液时,容量瓶未干燥_________;定容时俯视刻度线_________。