题目内容
7.NA代表阿伏加德罗常数.下列有关NA的叙述中,正确的是( )| A. | 在钠与氯气的反应中,1mol钠失去电子的数目为2NA | |
| B. | 14g氮气所含的氮原子数为NA | |
| C. | 标准状况下,22.4 L水所含的水分子数为NA | |
| D. | 1mol任何物质所含的分子数均为NA |
分析 A、根据反应后钠变为+1价来分析;
B、氮气由氮原子构成;
C、标况下,水为液体;
D、物质不一定由分子构成.
解答 解:A、反应后钠变为+1价,故1mol钠失去1mol电子即NA个,故A错误;
B、氮气由氮原子构成,故14g氮气中含有的氮原子的物质的量n=$\frac{14g}{14g/mol}$=1mol,即NA个,故B正确;
C、标况下,水为液体,不能根据气体摩尔体积来计算其物质的量,故C错误;
D、物质不一定由分子构成,还可能由原子或离子构成,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
11.下列关于“摩尔”的理解正确的是( )
| A. | 摩尔是国际科学界建议采用的一种物理量 | |
| B. | 我们把含有6.02×1023个粒子的任何粒子的集体计量为1摩尔 | |
| C. | 摩尔是表示物质的粒子个数的单位,简称摩,符号为mol | |
| D. | 1mol氧含6.02×1023个O2 |
15.某化学兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下系列实验.实验结果记录如下:
试根据表中的实验现象回答下列问题:
(1)实验1、2中Al所做的电极(正极或负极)不同(填“相同”或“不同”).
(2)实验3中,铝为负极,电极反应式:2Al-6e-═2Al3+.
(3)实验4中,铝作负极,理由是Al失去电子,写出铝电极的电极反应式Al-3e-+4OH-═AlO2-+2H2O.
(4)解释实验5中电流计偏向铝的原因Al遇浓硝酸发生钝化,发生Zn与浓硝酸的氧化还原反应,Zn作负极,Al作正极,电流由正极流向负极,所以电流计指针偏向铝.
| 编号 | 电极材料 | 电解质溶液 | 电液计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
(1)实验1、2中Al所做的电极(正极或负极)不同(填“相同”或“不同”).
(2)实验3中,铝为负极,电极反应式:2Al-6e-═2Al3+.
(3)实验4中,铝作负极,理由是Al失去电子,写出铝电极的电极反应式Al-3e-+4OH-═AlO2-+2H2O.
(4)解释实验5中电流计偏向铝的原因Al遇浓硝酸发生钝化,发生Zn与浓硝酸的氧化还原反应,Zn作负极,Al作正极,电流由正极流向负极,所以电流计指针偏向铝.
19.下列说法正确的是( )
| A. | 若高分子对应的单体只有一种,则此高聚物与单体一定有相同的最简式 | |
| B. | 等物质的量的乙烯与乙醇充分燃烧时消耗氧气的质量不相等 | |
| C. | 分子式为C6H12的某链状有机物,且6个碳原子一定在同一平面上,则与氢气加成后产物的名称为:2,3一二甲基丁烷 | |
| D. | 有机物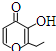 的一种芳香族同分异构体能发生银镜反应 的一种芳香族同分异构体能发生银镜反应 |
16.下列说法正确的是( )
| A. | 将(CH3)3CCH2Cl与氢氧化钾的乙醇溶液加热一段时间后冷却,再滴加硝酸酸化的硝酸银溶液,可观察到有白色沉淀产生 | |
| B. | 新制氢氧化铜悬浊液可检验失去标签的乙醛、乙酸、乙酸乙酯、葡萄糖溶液(必要时可加热) | |
| C. | 制备乙酸乙酯时加入试剂的顺序是,在一支试管中加入3mL浓硫酸,然后慢慢加入2mL无水乙醇和2mL无水乙酸 | |
| D. | 向淀粉溶液中加稀硫酸,加热几分钟,冷却后加入新制氢氧化铜悬浊液,若加热后未见砖红色沉淀生成 说明淀粉未开始水解 |
17.氢气是21世纪极有前途的新型能源,是各国研究的热点之一.氢能开发的首要问题是研究如何以水为原料制取氢气.以下研究方向中你认为可行的是( )
| A. | 大量建设水电站,用电力分解水制取氢气 | |
| B. | 利用核能,使水分解产生氢气 | |
| C. | 寻找更多的化石燃料,利用其燃烧放热,使水分解产生氢气 | |
| D. | 寻找特殊化学物质,用于开发廉价能源,以分解水制取氢气 |
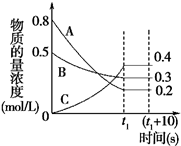 如图表示在一定的温度下,容积固定的密闭容器中,A、B、C三种气体物质的浓度随时间变化的情况,试回答下列问题:
如图表示在一定的温度下,容积固定的密闭容器中,A、B、C三种气体物质的浓度随时间变化的情况,试回答下列问题: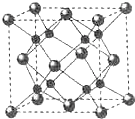 A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题: