题目内容
【题目】下列可以证明2HI(g)![]() H2(g)+I2(g)已达平衡状态的是( )
H2(g)+I2(g)已达平衡状态的是( )
①单位时间内生成nmolH2的同时生成nmolHI
②一个H—H键断裂的同时有两个H—I键断裂
③温度和体积一定时,混合气体密度不再变化
④v(H2)=v(I2)=0.5v(HI)
⑤c(HI):c(H2):c(I2)=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧温度和压强一定时,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
A. ②③④⑤⑥B. ②⑥⑦⑧⑨
C. ①②⑥⑧D. ②⑥⑨
【答案】D
【解析】
①单位时间内生成nmolH2的同时生成nmolHI,说明正反应速率大于逆反应速率,反应未达到平衡;
②H—H键断表示逆反应反向,H—I键断裂表示正反应方向,一个H—H键断裂的同时有两个H—I键断裂,表示正逆反应速率相等,可以说明反应达到平衡;
③温度和体积一定时,反应前后的体积不变,所以混合气体密度始终不变,所以不能说明反应达到平衡;
④v(H2)=v(I2)=0.5v(HI),没有说明反应的方向,故不能说明反应达到平衡;
⑤c(HI):c(H2):c(I2)=2:1:1,不能说明反应物或生成物浓度不再变化,不能说明反应达到平衡;
⑥温度和体积一定时,某一生成物浓度不再变化,说明某物质的生成速率等于其消耗速率,也就是正反应速率等于逆反应速率,能说明反应达到平衡;
⑦温度和体积一定时,反应前后气体体积不变,所以压强始终不变,故压强不变时,不能说明反应达到平衡;
⑧温度和压强一定时,反应前后气体的总物质的量不变,根据质量守恒,混合气体的平均相对分子质量始终不变,故混合气体的平均相对分子质量不再变化不能说明反应达到平衡;
⑨温度和体积一定时,混合气体中只有I2有颜色,所以颜色不变说明物质浓度不变,能说明反应达到平衡,
故选D。

【题目】下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
选项 | 实验 | 现象 | 结论 |
A | 乙酸乙酯与稀硫酸共热、搅拌 | 液体不再分层 | 乙酸乙酯在酸性条件下完全水解成可溶性物质 |
B | 向鸡蛋清溶液中加入饱和(NH4)2SO4溶液 | 生成白色沉淀 | 蛋白质发生了变性 |
C | 淀粉在稀硫酸的作用下水解后,加入新制Cu(OH)2后加热 | 有砖红色沉淀生成 | 淀粉已经完全水解 |
D | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 氧化性:Cl2>I2 |
A.AB.BC.CD.D
【题目】NF3(三氟化氮)在常温常压下是无色、无味的气体,是微电子工业中一种优良的等离子蚀刻气体。回答下列问题:
(1)NF3的电子式为______,N元素的化合价为______。
(2)F2与NH3直接反应生成NF3的化学方程式为______。
(3)实验室模拟工业上利用电解熔融NH4HF2(NH4FHF)法制取NF3,阳极为以Ni为基本材料的合金(内含其他金属,忽略镍及其他金属的反应),阴极为碳素钢,电解废液可回收再利用。
①电解时NF3在______极生成;阴极产生的气体是______(填化学式)。
②电解后废液(含Ni少量Fe和Cu的单质及NH4HF2等)可经如下流程进行回收再利用:
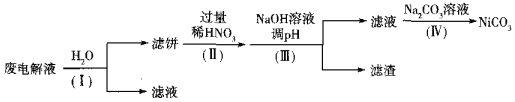
已知该实验条件下,部分金属离子开始沉淀与沉淀完全的pH如下表
金属离子 | Ni2+ | Fe2+ | Cu2+ | Fe3+ |
开始沉淀时的pH | 7.2 | 7.0 | 4.7 | 1.9 |
沉淀完全时的pH | 9.2 | 9.0 | 6.7 | 3.2 |
步骤I的目的是______;步骤Ⅱ滤饼中Ni溶于硝酸的离子方程式为______(HNO3的还原产物为NO);步骤Ⅲ调节pH时,理论上pH应控制的范围是______。