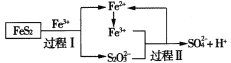
��Ŀ����
����Ŀ����2.56gCu��200mLijŨ�ȵ�ŨHNO3��ϣ����ŷ�Ӧ�Ľ��������������ɫ��dz����Cu��Ӧ��ȫʱ�����ռ�������1.12L(��״��)��
���й��ڸ÷�Ӧ�ķ���������ǣ� ��
A.�÷�Ӧ���ɵ�NO2��NO�������Ϊ7 : 3
B.�÷�Ӧת�Ƶ�����Ϊ0.04NA
C.�÷�Ӧ����HNO3�����ʵ���Ϊ0.13mol
D.��Ӧ������������Һ��(���Է�Ӧǰ����Һ����ı仯)c(NO3-) = 0.4 mol��L-1
���𰸡�BD
��������
ͭ�����ᷴӦ������Ũ�ȵļ��٣�����Ļ�ԭ����ļ�̬Խ�ͣ�ͭ��Ũ���ᷴӦ����NO2������ϡ���ᷴӦʱ������NO�������ɵ�������NO2��NO����n(NO2)+n(NO)=![]() =0.05mol��������ԭ����������ʵ���Ϊ0.05mol��n(Cu)=
=0.05mol��������ԭ����������ʵ���Ϊ0.05mol��n(Cu)=![]() =0.04mol��������n(Cu(NO3)2)=0.04mol����֪�������Ե���������ʵ���Ϊ0.04mol��2=0.08mol����μӷ�Ӧ����������ʵ���Ϊ��0.05mol+0.08mol=0.13mol��
=0.04mol��������n(Cu(NO3)2)=0.04mol����֪�������Ե���������ʵ���Ϊ0.04mol��2=0.08mol����μӷ�Ӧ����������ʵ���Ϊ��0.05mol+0.08mol=0.13mol��
A���ɷ���֪n(NO2)+n(NO)=0.05mol�����е���غ�n(NO2)��1+n(NO)��3= n(Cu)��2=0.08mol����ã�n(NO2)=0.35��n(NO)=0.15mol����÷�Ӧ���ɵ�NO2��NO�������Ϊ0.35mol��0.15mol=7 : 3����A��ȷ��
B��n(Cu)=![]() =0.04mol����÷�Ӧת�Ƶ�����Ϊ0.08NA����B����
=0.04mol����÷�Ӧת�Ƶ�����Ϊ0.08NA����B����
C���ɷ���֪�÷�Ӧ����HNO3�����ʵ���Ϊ0.13mol����C��ȷ��
D����Ӧ������������Һ�г����ɵ�Cu(NO3)2��������δ��Ӧ��HNO3����δ��Ӧ��HNO3�����ʵ���δ֪���������㷴Ӧ����Һ��c(NO3-)����D����
�ʴ�ΪBD��

����Ŀ����3�������Ϊ4.0 L�ĺ����ܱ������У���Ӧ CO2(g)��C(s)![]() 2CO(g) ��H > 0���ֱ���һ���¶��´ﵽ��ѧƽ��״̬������˵����ȷ����
2CO(g) ��H > 0���ֱ���һ���¶��´ﵽ��ѧƽ��״̬������˵����ȷ����
���� | �¶�/K | ��ʼʱ���ʵ���/mol | ƽ��ʱ���ʵ���/mol | ||
n(CO2) | n(C) | n(CO) | n(CO) | ||
I | 977 | 0.56 | 1.12 | 0 | 0.8 |
II | 977 | 1.12 | 1.12 | 0 | x |
III | 1250 | 0 | 0 | 1.12 | y |
A.977 K���÷�Ӧ�Ļ�ѧƽ�ⳣ��ֵΪ4
B.�ﵽƽ��ʱ��������I������C������ƽ�������ƶ�
C.�ﵽƽ��ʱ������I��CO2��ת���ʱ�����II�еĴ�
D.�ﵽƽ��ʱ������III�е�CO��ת���ʴ���28.6%
����Ŀ����.�������ڹ�ҵ�ϳɰ� N2(g) + 3H2(g) ![]() 2NH3(g)����H = -92.2 kJ��mol-1��һ���¶��£����ݻ��㶨���ܱ������У�һ������N2��H2��Ӧ�ﵽƽ��ı�ijһ�����������Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ������t5 �pt7ʱ������Ӧ��ʵ�������ı�ֱ���
2NH3(g)����H = -92.2 kJ��mol-1��һ���¶��£����ݻ��㶨���ܱ������У�һ������N2��H2��Ӧ�ﵽƽ��ı�ijһ�����������Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ������t5 �pt7ʱ������Ӧ��ʵ�������ı�ֱ���
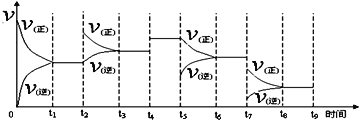
t5 ___________________��t7___________________��
��.��֪��ѧ��Ӧ�٣�Fe(s)+CO2(g) ![]() FeO(s)+CO(g), ��ƽ�ⳣ��ΪK1��
FeO(s)+CO(g), ��ƽ�ⳣ��ΪK1��
��ѧ��Ӧ�ڣ�Fe(s)+H2O(g) ![]() FeO(s)+H2(g)����ƽ�ⳣ��ΪK2��
FeO(s)+H2(g)����ƽ�ⳣ��ΪK2��
���¶�973K��1173K����£�K1��K2��ֵ�ֱ����£�
�¶� | K1 | K2 |
973K | 1.47 | 2.38 |
1173 | 2.15 | 1.67 |
��1��1173Kʱ����c(CO2)=2mol/L��c(CO) =5mol/L�����ʱ��Ӧ��ƽ����__________����������������������Ӧ�����ƶ���
��2�����з�Ӧ��CO2(g)+H2(g) ![]() CO(g)+H2O(g)��д���÷�Ӧ��ƽ�ⳣ��K3�ı���ʽ��K3=_______________________����K1 �� K2��ʾ�����ݴ˹�ϵʽ���ϱ����ݣ����ƶϳ���Ӧ����______��������������������������Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ��������Ӧ�����ƶ����ɲ�ȡ�Ĵ�ʩ��______(��д���)��
CO(g)+H2O(g)��д���÷�Ӧ��ƽ�ⳣ��K3�ı���ʽ��K3=_______________________����K1 �� K2��ʾ�����ݴ˹�ϵʽ���ϱ����ݣ����ƶϳ���Ӧ����______��������������������������Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ��������Ӧ�����ƶ����ɲ�ȡ�Ĵ�ʩ��______(��д���)��
A����С��Ӧ�����ݻ� B������Ӧ�����ݻ� C�������¶�
D�������¶� E��ʹ�ú��ʵĴ��� F���跨����CO����
���жϷ�Ӧ���Ѵ�ƽ��״̬����_______________________________��
A������������ѹǿ���� B�����������c(CO)����
C��![]() (H2)==
(H2)==![]() (H2O) D��c(CO2)==c(CO)
(H2O) D��c(CO2)==c(CO)
��3��723Kʱ��0.2molCO2��0.1molH2ͨ���յ�1L�����ܱ������У�������Ӧ�ۣ��ﵽƽ���ˮ�����ʵ�������Ϊ0.1����H2��ת��������H2��=___________����723K�÷�Ӧ��ƽ�ⳣ��ΪK=________________�������������λ��Ч���֣�