题目内容
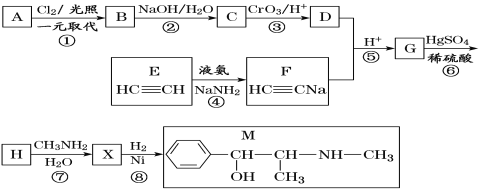
【题目】乙炔、乙烯均是重要的化工原料。回答下列问题:
(1)1902年,Sabatier首次发现,常压下过渡金属可以催化含有双键或叁键的气态烃的加氢反应。
①已知:C2H2(g)+H2(g)═C2H4(g)△H1=-174.3kJ·mol—1
K1(300K)=3.37×1024
C2H2(g)+2H2(g)=C2H6(g)△H2═-311.0kJ·mol一l
K2(300K)═1.19×1042
则反应C2H4(g)+H2(g)═C2H6(g)的△H=___kJ·mol一1,K(300K)=__(保留三位有效数字)。
②2010年Sheth等得出乙炔在Pd表面选择加氢的反应机理(如图)。其中吸附在Pd表面上的物种用*标注。

上述吸附反应为____(填“放热”或“吸热”)反应,该历程中最大能垒(活化能)为____kJ·mol-1,该步骤的化学方程式为____。
(2)在恒容密闭容器中充入乙烯,一定条件下发生反应C2H4(g)C2H2(g)+H2(g)。乙烯的离解率为a,平衡时容器内气体总压强为P总,则分压p(C2H4)═___(用p总和a表示)。
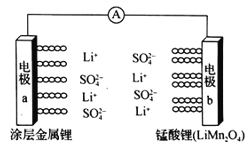
(3)用如图装置电解含CO2的某酸性废水溶液,阴极产物中含有乙烯。

该分离膜为___(填“阳”或“阴”)离子选择性交换膜;生成乙烯的电极反应式为___。
【答案】-136.7 3.53×1017 放热 +85 C2H3*+H*→C2H4* ![]() 阳 2CO2+12H++12e-=C2H4+4H2O
阳 2CO2+12H++12e-=C2H4+4H2O
【解析】
(1)①根据盖斯定律,△H2-△H1可得C2H4(g)+H2(g)═C2H6(g)的△H,K=![]() ;
;
②吸附时能量降低,解吸时能量升高,C2H3*+H*→C2H4*的活化能最大,为+85kJ·mol-1;
(2)根据三段式列式求解;平衡分压:p(C2H4)=n(C2H4)/n总 P总;
(3)阳极发生反应:2H2O一4e-=4H++O2↑,生成的H+向阴极移动,故用阳离子选择性交换膜,在阳极CO2得到电子结合H+生成一系列燃料,其中生成乙烯的电极反应为2CO2+12H++12e-=C2H4+4H2O。
(1)①C2H4(g)+H2(g)═C2H6(g)的△H=△H2-△H1=-136.7kJ·mol-1,300K时的平衡常数K=![]() =1.19×1042/3.37×1024=3.53×1017。
=1.19×1042/3.37×1024=3.53×1017。
②由图可知,吸附时能量降低,解吸时能量升高,如C2H4*→C2H4 △H=+82kJ·mol-1,基元反应中,C2H3*+H*→C2H4*的活化能最大,为+85kJ·mol-1。
(2)由反应:C2H4(g)![]() C2H2(g)+H2(g)
C2H2(g)+H2(g)
起始/mol n 0 0
转化/mol ![]()
![]()
![]()
平衡/mol ![]()
![]()
![]()
平衡时总物质的量:![]() ,
,
平衡分压:p(C2H4)=![]() 。
。
(3)阳极发生反应:2H2O一4e-=4H++O2↑,生成的H+向阴极移动,故用阳离子选择性交换膜,在阳极CO2得到电子结合H+生成一系列燃料,其中生成乙烯的电极反应为2CO2+

 口算小状元口算速算天天练系列答案
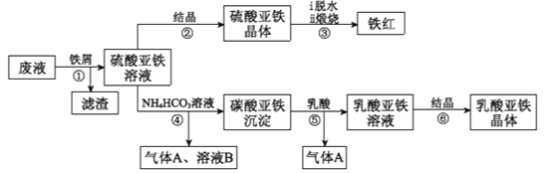
口算小状元口算速算天天练系列答案【题目】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下两种方法来制备无水FeCl2。有关物质的性质如下:
C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 | |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯,易溶于乙醇,易吸水 | ||
熔点/℃ | -45 | 53 | 易升华 | |
沸点/℃ | 132 | 173 | ---------------------- | -------------------- |
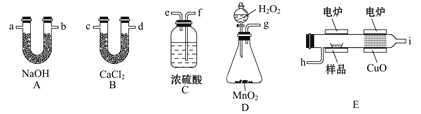
(1)H2还原无水FeCl3制取FeCl2。有关装置如图:
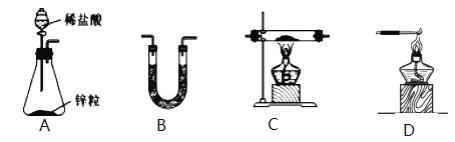
①H2还原无水FeCl3制取FeCl2的化学方程式为_____。
②按气流由左到右的方向,上述仪器的连接顺序为_____。(填字母,装置可多次使用);B中盛放的试剂是_____。
③该制备装置的缺点为_____。
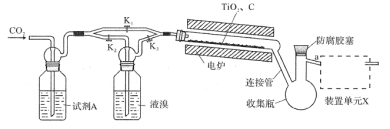
(2)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按如图装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。

①仪器a的作用是_____。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是_____,回收滤液中C6H5C1的操作是_____。
③反应后将锥形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol/L NaOH溶液滴定,终点时消耗NaOH溶液为19.60mL,则氯化铁的转化率为_____。
④为了减少实验误差,在制取无水FeCl2过程中应采取的措施有:_____(写出一点即可)。