题目内容
17.下列对应化学反应的离子方程式书写正确的是( )| A. | 氢氧化铁与盐酸反应:H++OH-═H2O | |
| B. | Ca(HCO3)2溶于稀盐酸中:CO32-+2H+═CO2↑+H2O | |
| C. | 铁与H2SO4反应:Fe+2H+═Fe3++H2↑ | |
| D. | 澄清的石灰水与醋酸反应:OH-+CH3COOH═CH3COO-+H2O |
分析 A.氢氧化铁为沉淀,保留化学式;
B.碳酸氢根离子为弱酸的酸式根离子,不能拆;
C.电荷不守恒;
D.生成醋酸钙和水.
解答 解:A.氢氧化铁与盐酸反应,离子方程式:3H++Fe(OH)3═3H2O+Fe3+,故A错误;
B.Ca(HCO3)2溶于稀盐酸中,离子方程式:HCO3-+H+═CO2↑+H2O,故B错误;
C.铁与H2SO4反应生硫酸亚铁,离子方程式:Fe+2H+═Fe2++H2↑,故C错误;
D.澄清的石灰水与醋酸反应,离子方程式:OH-+CH3COOH═CH3COO-+H2O,故D正确;
故选:D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,注意微溶物在书写离子方程式的拆分原则,题目难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
7.实验中需2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取NaCl的质量分别( )
| A. | 1000mL,117g | B. | 950mL,111.2 g | C. | 任意规格,117g | D. | 500mL,111.2g |
12.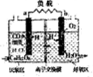 利用环境中细菌对有机质的催化降解能力,科学家开发出了微生物燃料电池,其装置如图,a、b为惰性电极,利用该装置将污水中的有机物(以C6H12O6为例)经氧化而除去,从而达到净化水的目的,下列说法不正确的是( )
利用环境中细菌对有机质的催化降解能力,科学家开发出了微生物燃料电池,其装置如图,a、b为惰性电极,利用该装置将污水中的有机物(以C6H12O6为例)经氧化而除去,从而达到净化水的目的,下列说法不正确的是( )
 利用环境中细菌对有机质的催化降解能力,科学家开发出了微生物燃料电池,其装置如图,a、b为惰性电极,利用该装置将污水中的有机物(以C6H12O6为例)经氧化而除去,从而达到净化水的目的,下列说法不正确的是( )
利用环境中细菌对有机质的催化降解能力,科学家开发出了微生物燃料电池,其装置如图,a、b为惰性电极,利用该装置将污水中的有机物(以C6H12O6为例)经氧化而除去,从而达到净化水的目的,下列说法不正确的是( )| A. | a电极反应式为:C6H12O6+6H2O-24e-═6CO2+24H+ | |
| B. | 反应过程中产生的质子透过阳离子交换膜扩散到好氧区 | |
| C. | 电流从右侧电极经过负载后流向左侧电极 | |
| D. | 常温下,用该电池电解一定量的饱和硫酸铜溶液(电极为惰性电极),其中水的电离平衡向左移动 |
2.某10% NaOH溶液,加热蒸发掉100g水后得到80mL 20% 的溶液,则该20% NaOH溶液的物质的量浓度为
( )
( )
| A. | 5.25 mol/L | B. | 12.5 mol/L | C. | 7.5 mol/L | D. | 6.25 mol/L |
9.足量铜溶于一定量浓硝酸,产生NO2、N2O4、NO的混合气体,这些气体若与1.12LO2(标准状况)混合后通入水中,气体被水完全吸收.若向原所得溶液中加入5mol•L-1H2SO4溶液100mL,则继续溶解的Cu的质量为( )
| A. | 6.4g | B. | 9.6g | C. | 19.2g | D. | 24g |
6.下列反应的离子方程式正确的是澄清的石灰水跟盐酸反应( )
| A. | 澄清的石灰水跟盐酸反应2H++Ca(OH)2═H2O+Ca2+ | |
| B. | 铁和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-═CO32-+H2O | |
| D. | 金属钠跟水反应:Na+2H2O═Na++2OH-+H2↑ |
7.下列试剂的贮存方法错误的是( )
| A. | 钠保存在煤油中 | |
| B. | 用带磨口玻璃塞的试剂瓶盛放NaOH溶液 | |
| C. | 存放液溴时需水封 | |
| D. | 保存氯化亚铁溶液时,要加入少量的铁粉 |
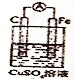 原电池实现了化学能与电能之间的转化,完成下列问题:
原电池实现了化学能与电能之间的转化,完成下列问题: