题目内容
【题目】2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户。用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是
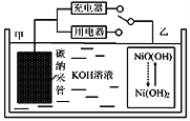
A. 放电时,乙电极反应为:Ni(OH)2+OH- e=NiO(OH)+H2O
B. 放电时,甲电极为正极,OH移向乙电极
C. 电池总反应为H2+2NiO(OH) ![]() 2Ni(OH)2
2Ni(OH)2
D. 充电时,电池的碳电极与直流电源的正极相连
【答案】C
【解析】A、放电时,负极失电子发生氧化反应,正极发生还原反应。根据示意图可知甲电极通入氢气,甲电极是负极,电极反应为H2-2e-+2OH-=2H2O,乙电极是正极,则乙中电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-,A错误;B、放电时,甲电极为负极,OH移向甲电极,B错误;C、根据以上分析可知电池总反应为H2+2NiO(OH)![]() 2Ni(OH)2,C正确;D、根据正接正,负接负,充电时,电池的碳电极与外电源的负极相连,D错误;答案选C。
2Ni(OH)2,C正确;D、根据正接正,负接负,充电时,电池的碳电极与外电源的负极相连,D错误;答案选C。

【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 900 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应逆反应的△H_____0(填“<”“>”“=”)。
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol·L-1·s-1。则6s时c(A)=_____________,C的物质的量为_____________;若反应经一段时间后,达到平衡时A的转化率为_______________,如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率为 ___________________。
(3)1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为____________。
A(g)+B(g)的平衡常数的值为____________。
