题目内容
根据元素周期律判断,下列递变规律不正确的是 ( )
| A.Na、Mg、Al的金属性依次减弱 |
| B.HCl、HBr、HI的稳定性依次增强 |
| C.HclO4、H2SO4、H3PO4的酸性依次减弱 |
| D.Li、Na、K分别与水反应的剧烈程度依次增强 |
B
Na、Mg、Al的金属性依次减弱,同周期元素自左至右金属性渐弱,故说法正确。

练习册系列答案
相关题目
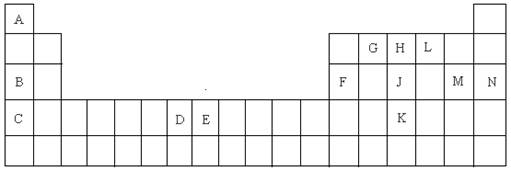
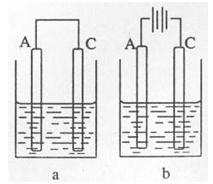
 H2(g)+CO2(g)
H2(g)+CO2(g)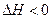 反应来制备合成氨的原料气,在1000℃下,用
反应来制备合成氨的原料气,在1000℃下,用 ,说明该元素与氧元素的非金属性的强弱______________________
,说明该元素与氧元素的非金属性的强弱______________________ __。
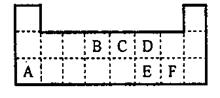
__。
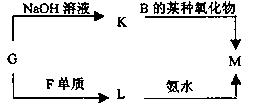
 化合物M是一种白色胶状沉淀,则M的化学式为 ;
化合物M是一种白色胶状沉淀,则M的化学式为 ; 子的电子层数
子的电子层数