题目内容
【题目】已知:
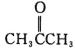
![]() ,
,![]() 为正四面体结构,其中P-P键的键能为
为正四面体结构,其中P-P键的键能为![]() ,
,![]() 的键能为
的键能为![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.该反应在任何温度下都能自发
B.![]() 和
和![]() 具有的总能量比
具有的总能量比![]() 具有的能量低
具有的能量低
C.![]() 的电子式为:
的电子式为:![]()
D.![]() 键的键能为
键的键能为![]()
【答案】D
【解析】
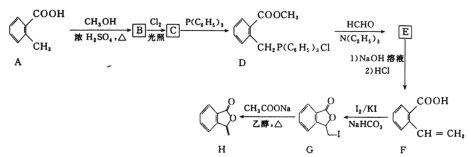
A.反应P4(s)+6Cl2(g)=4PCl3(g)△H1= -1266kJ·mol-1的△H<0、△S<0,由△G=△H-T△S可知,反应在高温度下反应不能自发进行,故A错误;
B.此反应是放热反应,则反应物的总能量大于生成物的总能量,即1molP4(s)和6molCl2(g)具有的总能量比4molPCl3(g)具有的能量高,故B错误;
C.PCl3是共价化合物,电子式中未参加成键的电子也要标出,则PCl3的电子式为![]() ,故C错误;
,故C错误;
D.已知P4(s)+6Cl2(g)=4PCl3(g)△H1= -1266kJ·mol-1=反应物的键能和-生成物的键能和,设P-Cl键的键能为xkJ·mol-1,则(198kJ·mol-1)×6+(243kJ·mol-1)×6 - x×12=-1266kJ·mol-1,解得:x=326,故D正确;
故答案为D。

练习册系列答案
相关题目
【题目】化学中很多规律![]() 性质
性质![]() 都有其适用范围,下列根据其推出的结论正确的是( )
都有其适用范围,下列根据其推出的结论正确的是( )
选项 | 规律 | 结论 |
A | 主族元素最高正化合价等于族序数 | 第ⅦA族元素最高正价都是+7 |
B | SO2和湿润的 | 二者混合后漂白性更强 |
C | 常温下铜与浓硝酸反应可以制取 | 常温下铁与浓硝酸反应也可以制取 |
D | 较强酸可以制取较弱酸 |
|
A.AB.BC.CD.D