题目内容
[2012·北京石景山一模](10分)我国制碱工业的先驱 侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:
侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:
NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3(晶体)
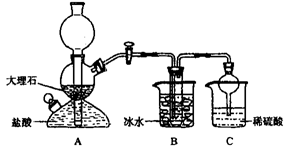
依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和。
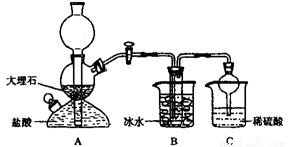
(1)A装置中所发生反应的离子方程式为 。
C装置中稀硫酸的作用为 。
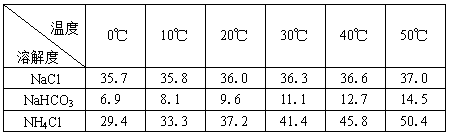
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
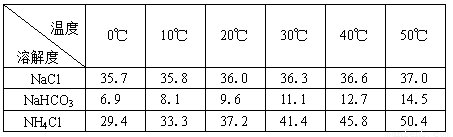
参照表中数据,请分析B装置中使用冰水的目的是 。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 装置之间(填写字母)连接一个盛有 的洗气装置,其作用是 。
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为 。
(10分)(1)CaCO3+2H+=Ca2++CO2↑+H2O 吸收从B装置中的试管内逸出的氨气,减少对环境的污染
(2)温度越低,碳酸氢钠的溶解度越小,便于析出
(3)A与B 饱和NaHCO3溶液(其他合理答案均给分) 除去CO2中混合的HCl气体
(4)60%
【解析】(4)NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3(晶体)
58.5 84
5.85g m
m=8.4g
所以NaHCO3的产率为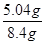 ×100%=60%。
×100%=60%。

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案 侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:
侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示: