��Ŀ����
300��ʱ����2mol A��2mol B������������2L�ܱ������У��������·�Ӧ��3A(g)+B(g) 2C(g)+2D(g) ��H��2minĩ�ﵽƽ�⣬����0.8mol D��
2C(g)+2D(g) ��H��2minĩ�ﵽƽ�⣬����0.8mol D��
(1)��2minĩʱ��A��ƽ��Ũ��Ϊ_____________��B��ת����___________��0-2min��D��ƽ����Ӧ����Ϊ_____________��
(2)�÷�Ӧ��ƽ�ⳣ������ʽΪ��K=_____________�����¶��µĻ�ѧƽ�ⳣ����ֵΪ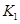 =____________��
=____________��
��֪350��ʱ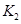 =l�����H________0���>����<������
=l�����H________0���>����<������
(3)��300��ʱ�����÷�Ӧ����ѹ�����ΪlL����A��ת����___________�����������С�����䡱����ԭ����__________________���������µ�ƽ�ⳣ��Ϊ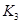 �� ��K3________
�� ��K3________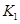 �����<����>����=������ԭ����_______________________��
�����<����>����=������ԭ����_______________________��
(4)���жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������__________________����ѡ�۷֣���
A��������ѹǿ���� B�����������c(A)����
C��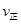 (A)=
(A)=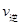 (C) D����������ܶȲ���
(C) D����������ܶȲ���
��1��0.4mol�ML 20�G 0.2 mol�M(L��min) (2)K={C2(C)C2(D) }�M{C3(A)C (B)} 0.5 >
(3)���䡣����ѹǿ��ƽ�ⲻ�ƶ�= Kֵֻ���¶��й� �� ��4��B
�������������(1)���ݷ�Ӧ����ʽ��3A(g)+B(g) 2C(g)+2D(g)�ɿ�������ӦʱA ��B��C��D�����ʵ����Ĺ�ϵ��3��1��2��2����Ϊ����0.8mol��D����������A1.2mol������B0.4mol������C0.8mol����A��ƽ��Ũ��Ϊ����2-1.2��mol��2L="0.4mol�ML" . B��ת����Ϊ��0.4mol��2mol�� 100%="20%," 0-2min��D��ƽ����Ӧ����ΪV="��C�M" ��t="(0.8mol��2L)" �M2min=" 0.2" mol�M(L��min).(2)��ѧƽ�ⳣ���ǿ��淴Ӧ�ﵽ��ѧƽ��ʱ��������Ũ����ָ���Ļ������Ӧ��Ũ����ָ���Ļ�֮K={C2(C)C2(D) }�M{C3(A)C (B)}���ﵽ��ѧƽ��ʱ�����ʵ�Ũ�ȷֱ���C(A)=" 0.4mol�ML" ;C(B)="(2-0.4)mol��2L=0.8mol�ML" ;C(C)=" 0.8mol" ��2L="0.4" mol�ML ;C(D)=" 0.8mol" ��2L="0.4" mol�ML�����Ի�ѧƽ�ⳣ��Ϊ��K1={��0.4��2����0.4��2}�M{��0.4��3��0.8}=0.5.����Ϊ��350��ʱK2=l���ɼ������¶ȣ�K����˵�������¶Ȼ�ѧƽ��������Ӧ�����ƶ������ݻ�ѧƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ���������Ӧ�����ȷ�Ӧ���ʡ�H>0.��3������Ӧ�������ѹ����Ҳ��������ѹǿ�����ݻ�ѧƽ���ƶ�ԭ��������ѹǿ����ѧƽ�������������С�ķ����ƶ������÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ����������ѹǿ����ѧƽ�ⲻ�ƶ�����ʱA��B��ת�����ʶ����ᷢ���仯����ѧƽ�ⳣ��ֻ���¶��йء���������Ͷ�ϵĶ��ټ������ء�����K1=K3. (4)����Ӧ�ﵽ��ѧƽ��ʱ�����ʵ�Ũ�Ȳ��䣬��ͬһ���ʱ�ʾ������Ӧ���ʺ��淴Ӧ������ȣ������ʵĺ������䡣����������������䣬�÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ�������κ�ʱ��ѹǿ���䣬������ܶ�Ҳ���䣬�����Dz�����Ϊ�ж�ƽ��ı�־����ȷѡ��Ϊ��B��
2C(g)+2D(g)�ɿ�������ӦʱA ��B��C��D�����ʵ����Ĺ�ϵ��3��1��2��2����Ϊ����0.8mol��D����������A1.2mol������B0.4mol������C0.8mol����A��ƽ��Ũ��Ϊ����2-1.2��mol��2L="0.4mol�ML" . B��ת����Ϊ��0.4mol��2mol�� 100%="20%," 0-2min��D��ƽ����Ӧ����ΪV="��C�M" ��t="(0.8mol��2L)" �M2min=" 0.2" mol�M(L��min).(2)��ѧƽ�ⳣ���ǿ��淴Ӧ�ﵽ��ѧƽ��ʱ��������Ũ����ָ���Ļ������Ӧ��Ũ����ָ���Ļ�֮K={C2(C)C2(D) }�M{C3(A)C (B)}���ﵽ��ѧƽ��ʱ�����ʵ�Ũ�ȷֱ���C(A)=" 0.4mol�ML" ;C(B)="(2-0.4)mol��2L=0.8mol�ML" ;C(C)=" 0.8mol" ��2L="0.4" mol�ML ;C(D)=" 0.8mol" ��2L="0.4" mol�ML�����Ի�ѧƽ�ⳣ��Ϊ��K1={��0.4��2����0.4��2}�M{��0.4��3��0.8}=0.5.����Ϊ��350��ʱK2=l���ɼ������¶ȣ�K����˵�������¶Ȼ�ѧƽ��������Ӧ�����ƶ������ݻ�ѧƽ���ƶ�ԭ���������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ���������Ӧ�����ȷ�Ӧ���ʡ�H>0.��3������Ӧ�������ѹ����Ҳ��������ѹǿ�����ݻ�ѧƽ���ƶ�ԭ��������ѹǿ����ѧƽ�������������С�ķ����ƶ������÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ����������ѹǿ����ѧƽ�ⲻ�ƶ�����ʱA��B��ת�����ʶ����ᷢ���仯����ѧƽ�ⳣ��ֻ���¶��йء���������Ͷ�ϵĶ��ټ������ء�����K1=K3. (4)����Ӧ�ﵽ��ѧƽ��ʱ�����ʵ�Ũ�Ȳ��䣬��ͬһ���ʱ�ʾ������Ӧ���ʺ��淴Ӧ������ȣ������ʵĺ������䡣����������������䣬�÷�Ӧ�Ǹ���Ӧǰ�����������ȵķ�Ӧ�������κ�ʱ��ѹǿ���䣬������ܶ�Ҳ���䣬�����Dz�����Ϊ�ж�ƽ��ı�־����ȷѡ��Ϊ��B��
���㣺���黯ѧ��Ӧ���ʼ���ѧƽ���������й�֪ʶ��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д���֪�ظ����(K2Cr2O7)��һ����Ҫ�ĵ����Լ���
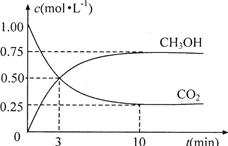
��1��ǿ�����Ե�K2Cr2O7��Һ�У���������ƽ�⣺ Cr2O72-����ɫ����H2O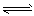 2CrO42-����ɫ����2H+��
2CrO42-����ɫ����2H+��
����Ҫʹ��Һ�ij�ɫ������пɲ��õķ����� ��
| A����������ϡ���� | B����������ϡ���� | C�����������ռ���� | D����ˮϡ�͡� |
ijѧ��Ϊ��̽��п�����ᷴӦ���������ʱ仯����100mLϡ�����м���������п�ۣ���״���²�������ۼ�ֵ���£�
| ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
| ���������mL�� | 50 | 120 | 232 | 290 | 310 |
��1����0��1��1��2��2��3��3��4��4��5 minʱ����У���Ӧ��������ʱ����� ��
ԭ��Ϊ ����Ӧ������С��ʱ����� ��
ԭ��Ϊ ����2����2��3minʱ����ڣ��������Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ ��
��3��Ϊ�˼�����Ӧ���ʵ������ٲ��������������������зֱ����������������Һ��A .����ˮ B .Na2SO4��Һ C. NaNO3��Һ D. CuSO4��Һ E. Na2CO3 ��Һ, ����Ϊ���е��� ��
 CH3OH(g)+H2O(g)����ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ��mol��1)�ı仯��
CH3OH(g)+H2O(g)����ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ��mol��1)�ı仯��
 2SO3(g)����H < 0�������淴Ӧ���ʵ�Ӱ����ͼ��ʾ��
2SO3(g)����H < 0�������淴Ӧ���ʵ�Ӱ����ͼ��ʾ��
 pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C������������С����
pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C������������С���� xC(g)������������̶�Ϊ2L����Ӧ1minʱ���ʣ��1.8molA��C��Ũ��Ϊ0.4mol/L������д���пհף�
xC(g)������������̶�Ϊ2L����Ӧ1minʱ���ʣ��1.8molA��C��Ũ��Ϊ0.4mol/L������д���пհף�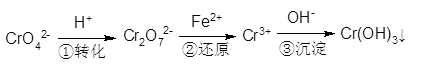
 Cr2O72-(��ɫ)+H2O
Cr2O72-(��ɫ)+H2O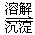 Cr3+(aq)+3OH��(aq)
Cr3+(aq)+3OH��(aq) CO(g)+H2(g)?131.4 kJ��
CO(g)+H2(g)?131.4 kJ��