题目内容
【题目】化合物X是一种药物合成的中间体,其结构简式如图所示。下列有关化合物X的说法正确的是( )
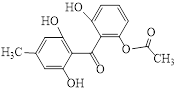
A. 化合物X的分子式为C16H16O6
B. 能发生加成反应、取代反应、消去反应
C. 1mol化合物X最多可与5molNaOH、7mol H2、4molBr2发生反应
D. 可与FeCl3溶液发生显色反应,但不能发生氧化反应
【答案】C
【解析】根据结构简式可知分子式为C16H14O6,A错误;酚羟基不能发生消去反应,B错误;酚羟基,酚酯都能和NaOH反应,共消耗5molNaOH,苯环、酮羰基均与氢气发生加成反应,共消耗7mol H2,酚羟基存在的情况下,苯酚发生邻对位取代反应,共消耗4molBr2,C正确;有机物可以发生燃烧氧化,D错误;正确选项C。

 阅读快车系列答案
阅读快车系列答案【题目】碳及其化合物在研究和生产中有许多重要用途.请回答下列问题:
(1)基态碳原子核外电子有__种空间运动状态,其价电子排布图为__.
(2)光气的分子式为COCl2,又称碳酰氯,是一种重要的含碳化合物,判断其分子立体构型为__,其碳原子杂化轨道类型为_____杂化.
(3)碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,如下表所示:
碳酸盐 | MgCO3 | CaCO3 | BaCO3 | SrCO3 |
热分解温度/℃ | 402 | 900 | 1172 | 1360 |
阳离子半径/pm | 66 | 99 | 112 | 135 |
试解释为什么随着阳离子半径的增大,碳酸盐的分解温度逐步升高?。 ______________
(4)碳的一种同素异形体﹣﹣C60,又名足球烯,是一种高度对称的球碳分子.立方烷(分子式:C8H8结构是立方体:![]() 是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如图所示,立方烷分子填充在原C60晶体的分子间八面体空隙中.则该复合型分子晶体的组成用二者的分子式可表示为__。
是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如图所示,立方烷分子填充在原C60晶体的分子间八面体空隙中.则该复合型分子晶体的组成用二者的分子式可表示为__。

(5)碳的另一种同素异形体——石墨,其晶体结构如图所示,则石墨晶胞含碳原子个数为__个.已知石墨的密度为ρg·cm﹣3,C﹣C键长为rcm,阿伏加德罗常数的值为NA,计算石墨晶体的层间距为__cm.
(6)金刚石和石墨的物理性质差异很大,其中:熔点较高的是___________,试从结构分析___________;硬度大的是___________,其结构原因是___________。


